Iodo: propriedades químicas, a fórmula, o número na tabela Periódica
Álcool solução de iodo ... Desde a infância, familiar a todas as crianças e seus pais assistente ao comprador, ссадинах e порезах. Ele é rápido e eficiente, прижигающим e desinfetante ferida. No entanto, o âmbito de aplicação de uma substância não se limita apenas a medicina, т. к. propriedades químicas de iodo são muito variadas. O objetivo de nosso artigo – familiarizar-se com eles para mais informações.

Característica Física
Uma Simples substância tem aparência azul-violeta de cristal. Quando aquecido, devido às características da estrutura interna da grade cristalina, e é de ter em seus sites de moléculas, a conexão não é derretido, e logo forma um par. É возгонка ou sublimação. Ela explica a fraca comunicação entre as moléculas dentro do cristal, que facilmente se desprender do outro – formada gasoso fase de uma substância. O número de iodo na tabela Periódica – 53. E a sua posição entre os outros elementos químicos indica afiliação à неметаллам. Detenhamo-nos neste assunto por diante.
O Lugar do elemento na tabela periódica
O Iodo está no quinto período, VII grupo e, juntamente com o flúor, o cloro, o bromo e o астатом forma um subgrupo de halogéneo. Com o aumento da carga do kernel e atômico, raio os representantes de halogéneo, ocorre o enfraquecimento não metálicos, propriedades, portanto, o iodo menos ativo do que o cloro ou bromo, e sua electronegatividade dos também abaixo. Massa atômica de iodo 126,9045. Simples substância apresentado двухатомными moléculas e livre de halogênio. A seguir iremos explorar com a construção de um átomo de um elemento.
Mais:
A história do desenvolvimento da tecnologia de computação
Os primeiros dispositivos de computação foram os próprios dedos de uma pessoa. Quando a ferramenta foi suficiente, no curso de iam pedras, galhos, conchas. Dobrando-se de um conjunto de dezenas, depois centenas, o homem aprendeu a contar e usar as fe...
O impulso nervoso, a sua conversão e o mecanismo de transmissão
O sistema Nervoso humano atua como uma espécie de coordenador no nosso corpo. Ela passa o comando do cérebro musculatura, órgãos, tecidos e processa os sinais de longo alcance deles. Como uma espécie de suporte de dados, é usado o impulso nervoso. O ...
Canal do panamá: um ano, a abertura oficial do objecto e a sua importância histórica
Durante séculos, a humanidade tenta recriar condições naturais da Terra, com o objetivo de receber quaisquer benefícios. Um desses casos, a adaptação é do canal do Panamá, o ano, a abertura oficial deste objeto foi marcado por um evento, повлиявшим p...
Características de fórmulas
Os Cinco níveis de energia e quase totalmente preenchido por elétrons último deles, confirmam a presença de um elemento de características marcantes неметаллов. Como outros halogênios, o iodo é um forte oxidante, tirando os metais e dos não-metálicos e de elementos - o enxofre, o carbono, o nitrogênio - em falta antes de completar o quinto nível, o elétron.
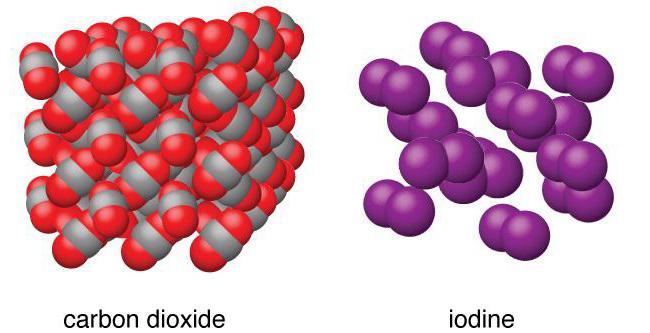
Iodo – metalóide, em que as moléculas está presente total do par p-tron, que liga os átomos entre si. Sua densidade no local de um templo maior, comum a nuvem de elétrons não desloca-se a qualquer um dos átomos e localiza-se no centro da molécula. Formado неполярная ковалентная comunicação, e a própria molécula tem uma forma linear. Na série livre de halogênio, de flúor até астата, a força de ligação covalent diminui. Pode ocorrer a diminuição do entalpia, da qual depende a desintegração das moléculas de um item de átomos. Que conseqüências para as propriedades químicas de iodo tem?
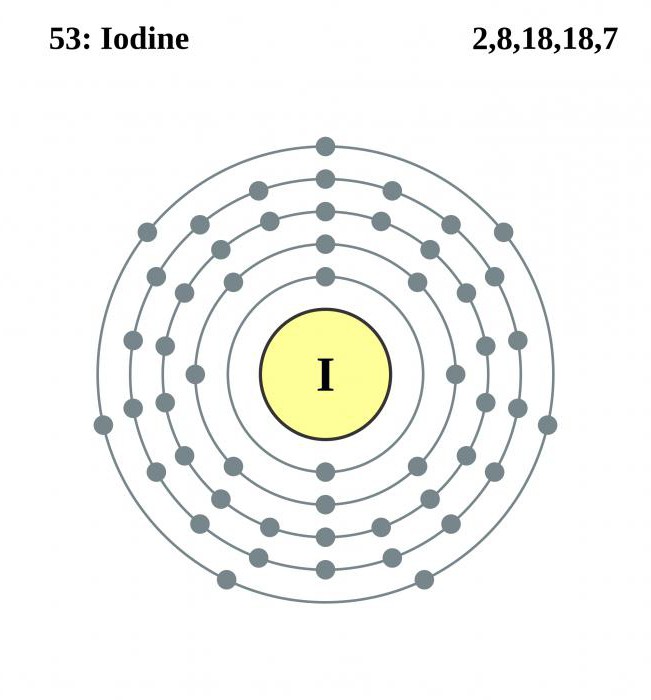
Por que a atividade de iodo é menor que a de outros halogênios
Reactividade неметаллов determinada força que os nós são atraídos para o núcleo do próprio átomo externos de elétrons. Quanto menor o raio de um átomo, maior a força eletrostática de atração-lo negativamente carregadas de partículas de outros átomos acima. Quanto maior o número do período em que o item está localizado, mais níveis de energia, ele vai ter. O iodo está no quinto período, e a quantidade de energia camadas ele tem a mais que o bromo, cloro e flúor. É por isso que a molécula de iodo contém átomos com um raio muito maior do que anteriormente listados livre de halogênio. É por isso que as partículas I2 mais fraco atraem os elétrons, o que leva a um enfraquecimento de sua não-metálicos de propriedades. Estrutura interna da substância, inevitavelmente, a influência de suas características físicas. Dê exemplos concretos.

A Sublimação e a solubilidade
A Redução mútua de nós são atraídos átomos de iodo em sua molécula leva, como dissemos anteriormente, a um enfraquecimento da força covalent неполярной de comunicação. Ocorre diminuição da estabilidade da conexão à alta temperatura e aumentar o índice de dissociação térmica de suas moléculas. Uma característica distintiva de halogéneo: transferência da substância durante o aquecimento do estado sólido diretamente em gás, т. е. a sublimação é a principal característica física de iodo. A sua solubilidade em solventes orgânicos, por exemplo сероуглероде, бензоле, etanol, maior do que na água. Assim, em 100 g de água a 20 °pode dissolver a apenas 0,02 g da substância. Esta característica no laboratório utilizado para a extração de iodo solução aquosa. Взболтав-lo com um pouco de H2S, pode-se observar coloração violeta de sulfeto de hidrogênio, devido a transição nele moléculas de halogéneo.
Propriedades Químicas de iodo
Interagem com os metais, o elemento se comporta sempre da mesma maneira. Ele atrai валентные os elétrons do átomo do metal, que estão ou no último energia, camada (s-itens, tais como sódio, cálcio, lítio e т. д.), ou a penúltima camada que contém, por exemplo, d-os elétrons. Estes incluem o ferro, o manganês, o cobre e outros. Nestas reações o metal é um restaurador, iodo, cuja fórmula química I2, - oxidante. Portanto, é esta a alta atividade simples de uma substância é a razão de sua interação com muitos metais.
Merece atenção é a interação de iodo com a água durante o aquecimento. Em ph alcalino reação passa com a formação de uma mistura de йодидной e иодноватой ácidos. A última substância mostra as propriedades de um ácido forte e durante a desidratação se transforma em пятиокись de iodo. Se a mesma solução подкислить, produtos de reação interagem entre si, com a formação de origemsubstâncias – as moléculas livres I2 e água. Esta resposta refere-se à na восстановительному tipo, em que se manifestam as propriedades químicas de iodo como um forte oxidante.
De alta Qualidade a reação do amido
Como inorgânica e química orgânica, há um grupo de reações através das quais se pode identificar nos produtos da interação de determinados tipos simples ou complexos de íons. Para a detecção de macromoléculas hidrato de carbono complexo – amido - frequentemente 5% de álcool a solução I2. Por exemplo, para o corte bruto batatas pingando algumas de suas gotas, e a coloração da solução se torna azul. O mesmo efeito assistimos ao acerto de uma substância qualquer крахмалосодержащий produto. Esta reação, em resultado do que acontece azul iodo, é amplamente aplicado em química orgânica para a confirmação da presença do polímero na mistura pesquisada.
Sobre minerais propriedades de interação do produto de iodo e amido conhecido por muito tempo. Ele usou na ausência de antimicrobiais медикаментозных de medicamentos para o tratamento da diarréia, úlceras de estômago em estado de remissão, doenças do sistema respiratório. A ampla disseminação de крахмальный клейстер, contém cerca de 1 colher de chá de álcool de solução de iodo em 200 ml de água, recebeu por causa de ingredientes de baixo custo e facilidade de cozimento.
No Entanto, é preciso lembrar que o azul é o iodo é contra-indicado na terapia de crianças pequenas, pessoas que sofrem de hiper-sensibilidade a йодосодержащим medicamentos e doente базедовой doença.
Como nos não-metais reagem entre si
Entre os elementos do principal subgrupos VII grupo com iodo reage flúor ã o mais ativo do metalóide, o detentor do grau de oxidação. O processo é executado em tempo frio e acompanhado de uma explosão. Com o hidrogênio I2 interage com o forte aquecimento, e não até o final, produto da reação – HI - começa a decompor-se na origem da substância. Йодоводородная ácido forte o suficiente, e apesar de suas características semelhante ao хлоридную ácido, ainda demonstra mais pronunciados sinais de reserva. Como pode ser visto, propriedades químicas de iodo resultou da sua filiação ao ativo неметаллам, no entanto, o item é inferior a capacidade oxidativa брому, cloro e, claro, constitutivo do.

A Função de um elemento em organismos vivos
O Maior conteúdo de íons I o Nos tecidos da glândula tireóide, onde eles fazem parte de um тиреотропных de hormônios: tiroxina e triiodotironina. Eles regulam o crescimento e o desenvolvimento de tecido ósseo, a realização de impulsos nervosos, a velocidade do metabolismo. Especialmente perigoso é a falta de йодсодержащих de hormônios na infância, assim como pode haver um atraso mental, de desenvolvimento e o surgimento dos sintomas dessa doença, como o cretinismo.
A Falta de secreção de tiroxina em adultos relacionado com a deficiência de iodo na água e alimentos. Ela é acompanhada de queda de cabelo, formação de edema, diminuição da atividade física. O excesso do elemento no corpo também é extremamente perigoso, pois se desenvolve базедова a doença, os sintomas que – excitabilidade do sistema nervoso, tremores de extremidades, acentuado исхудание.
Alto teor de compostos de iodo é detectado alguns representantes do mundo da flora. As plantas mais baixas – - marrom e algas vermelhas - acumulam-los em seu талломе. Entre as plantas superiores рекордсменами de acúmulo de iodo são cereja, caqui, tâmaras e beterraba. Um grande número de elementos contém frutos do mar e peixes de água salgada.

Distribuição йодидов na natureza e formas de obtenção de pura substância
A Principal a massa de um elemento presente nos organismos vivos e máscaras Terra – гидросфере e литосфере - a associada estado. Sal de um elemento é a água do mar, mas a sua concentração é desprezível, de modo a extrair o puro iodo dela não é rentável. Muito mais eficiente para a obtenção de uma substância a partir de cinzas de algas marrons: фукуса, algas, саргассума.
Em escala industrial I2 destacam das águas subterrâneas em processos de extração de petróleo. A reciclagem de alguns minérios, por exemplo chilena de amônia, nela se encontram иодаты e гипоиодаты de potássio, dos quais, no futuro, extraído de um puro iodo. Bastante eficaz na redução de custos a receber I2 a partir de uma solução йодоводорода, de oxidação-lo com cloro. Recebida a conexão é uma importante matéria-prima para a indústria farmacêutica.
Além do já conhecido de 5% de solução alcoólica de iodo, contém não apenas uma simples matéria, mas e o sal – иодид de potássio, bem como o álcool e a água, em endocrinologia, por motivos de saúde aplicam as drogas tais como "o Iodo-ativo" e "Йодомарин".

Em áreas com baixo teor de compostos naturais, além de iodado sal, você pode usar esse remédio, como "Антиструмин". Ele contém a substância – iodeto de potássio - e recomendado como profilático do medicamento, utilizado para evitar os sintomas de эндемического bócio.
Article in other languages:
KK: https://tostpost.com/kk/b-l-m/12176-yod-himiyaly-asiet-formulasy-n-m-r-kestede-mendeleev.html
TR: https://tostpost.com/tr/e-itim/12177-yot-kimyasal-zellikleri-form-l-tablo-periyodik.html
UK: https://tostpost.com/uk/osv-ta/12172-yod-h-m-chn-vlastivost-formula-nomer-tablic-mendel-va.html

Alin Trodden - autor do artigo, editor
"Olá, sou o Alin Trodden. Escrevo textos, leio livros e procuro impressões. E eu não sou ruim em falar sobre isso. Estou sempre feliz em participar de projetos interessantes."
Notícias Relacionadas
Falar sobre a expressão "no entanto"
Muitas pessoas, depois de se formar na escola, saem de lá безграмотными. E não se trata de um mau professor, e uma preguiça. Mas nem todas as crianças sem exceção, o c, em qualquer sala de aula foram хорошисты. Mas, infelizmente, ...
Uma história sobre o verão idéias interessantes, plano e recomendações
Apesar do fato de que a história pro verão sugere a livre expressão de seus pensamentos e não prevê algum tipo específico de conhecimento, para muitos esse tipo de trabalho são dadas, não é fácil. Afinal, como é possível escrever ...
A definição do absolutismo. O estabelecimento do absolutismo, suas características
a Maioria dos livros de história oferecem aproximadamente a mesma definição do absolutismo. Esta ordem política formou na maioria dos países europeus dos séculos XVII-XVIII вв. É caracterizada por exclusiva autoridade do monarca, ...
O início da Segunda guerra mundial: as principais causas
a Mais épica, sangrenta e terrível guerra da história da humanidade, recebeu o nome da Segunda guerra mundial, começou não 1 de setembro de 1939, o dia, quando a Alemanha nazista atacou a Polônia. O início da Segunda guerra mundia...
o bloqueio Continental – é uma medida de restrição ou proibição da importação de certos tipos de produtos. Desde o início do século 19, começou uma reforma séria no campo econômico, muitos países da Europa. Os processos inte...
A composição do petróleo e propriedades do petróleo
Petróleo – é oleoso e líquido inflamável, o que é comum na zona осадочной shell a crosta da terra. Ela é uma das mais importantes minerais para o homem. O petróleo é um complexo composto цикланов, touros arènes e алкан...




















Comentários (0)
Este artigo possui nenhum comentário, seja o primeiro!