Now - 18:26:17
Атам у хіміі - гэта... Мадэль атама. Будова атама
Думкі аб сутнасці ўсяго навакольнага пачалі наведваць чалавецтва задоўга да моманту росквіту сучаснай цывілізацыі. Спачатку людзі разважалі пра існаванне нейкіх вышэйшых сіл, якія, як яны лічылі, якая прадвызначае ўсе быццё. Але ўжо даволі хутка філосафы і святары пачалі задумвацца над тым, з чаго, уласна, складаецца сама тканіна гэтага быцця. Тэорый было мноства, але ў гістарычнай перспектыве пануючай стала атамарнага.
 Што такое атам у хіміі? Гэта, а таксама ўсе спадарожныя тэмы мы абмяркуем у рамках дадзенага артыкула. Спадзяемся, што ў ёй вы знойдзеце адказы на ўсе пытанні, якія цікавяць вас пытанні.
Што такое атам у хіміі? Гэта, а таксама ўсе спадарожныя тэмы мы абмяркуем у рамках дадзенага артыкула. Спадзяемся, што ў ёй вы знойдзеце адказы на ўсе пытанні, якія цікавяць вас пытанні.
Родапачынальнік атамарна тэорыі
З чаго пачынаецца першы ўрок хіміі? Будова атама – вось галоўная тэма. Вы, напэўна, памятаеце, што слова «атам» перакладаецца з старажытнагрэцкай мовы як «непадзельны». Зараз многія гісторыкі лічаць, што першым высунуў тэорыю, гласившую аб нейкіх драбнюткіх часціцах, з якіх складаецца ўсё існае, Дэмакрыт. Ён жыў яшчэ ў пятым стагоддзі да нашай эры.
Да вялікі жаль, аб гэтым выбітным мысьляра практычна нічога не вядома. Да нас не дайшоў ні адзін пісьмовы крыніца тых часоў. А таму аб ідэях найвялікшага вучонага свайго часу нам даводзіцца пазнаваць выключна з прац Арыстоцеля, Платона, а таксама іншых старажытнагрэцкіх мысляроў.
такім чынам, наша тэма - "Будова атама". Па хіміі не ўсе мелі высокія ацэнкі, але многія памятаюць аб тым, што ўсе высновы старажытных навукоўцаў былі пабудаваныя выключна на высновах. Дэмакрыт выключэннем не быў.
Як разважаў Дэмакрыт?
Логіка яго была гранічна простая, але разам з тым геніяльная. Уявіце, што ў вас ёсць самы востры нож ва ўсім свеце. Вы бераце яблык, да прыкладу, а затым пачынаеце яго разрэзаць на дзве палоўкі, на чвэртачкі, іх зноў дзяліце... Словам, рана ці позна вы атрымаеце лусты такой мізэрнай таўшчыні, што далей іх дзяліць ужо будзе нельга. Вось гэта і будзе непадзельны атам. У хіміі гэта зацвярджэнне лічылася сапраўдным ледзь ці не да канца 19 стагоддзя.
Ад Дэмакрыта да сучасным уяўленням
Варта заўважыць, што ад старажытнагрэцкіх уяўленняў аб мікрасвеце захавалася адно толькі слова «атам». Цяпер кожны школьнік ведае, што навакольны нас свет складаецца з куды больш фундаментальных і дробных часціц. Акрамя таго, з пункту гледжання сучаснай навукі тэорыя Дэмакрыта была не больш чым чыста гіпатэтычнай выкладкай, не падмацаванай роўным лікам ніякімі доказамі. Зрэшты, у тыя часы не было электронных мікраскопаў, так што даказаць сваю правату іншымі спосабамі ў мысляра б усё роўна не атрымалася.
Больш:
Нервовы імпульс, яго пераўтварэнне і механізм перадачы
Нервовая сістэма чалавека выступае своеасаблівым каардынатарам у нашым арганізме. Яна перадае каманды ад мозгу мускулатуры, органаў, тканін і апрацоўвае сігналы, якія ідуць ад іх. У якасці своеасаблівага носьбіта дадзеных выкарыстоўваецца нервовы імп...
Куды паступаць пасля 11 класа? Якую выбраць прафесію?
Пры выбары сваёй будучай прафесіі не варта абапірацца на чые-то рэкамендацыі і парады, тым больш не трэба падпарадкоўвацца сваім бацькам, якія даволі часта вырашаюць без вас самастойна, куды паступіць пасля 11 класа. Варта задумацца, наколькі паспяхо...
Крывяносная сістэма жывёл, як вынік эвалюцыйнага развіцця свету
Крывяносная сістэма жывёл прайшла доўгі шлях фарміравання ў ходзе эвалюцыйнага развіцця свету. Яна ўтварылася на месцы рудыментарных частак першаснай паражніны цела, якая ў вышэйшых жывёл была выцесненая целломом, або другаснай паражніной цела. У пра...
Першыя падазрэнні аб тым, што Дэмакрыт на самай справе мае рацыю, з'явіліся ў хімікаў. Яны хутка выявілі, што многія рэчывы ў ходзе рэакцый распадаюцца на больш простыя кампаненты. Акрамя таго, менавіта хімікі вывелі строгія заканамернасці дадзеных працэсаў. Так, яны звярнулі ўвагу, што для атрымання вады патрабуецца восем масавых доляй кіслароду і адна - вадароду (закон Авагадра).
У Сярэднія стагоддзі любы матэрыялістычнае вучэнне, у тым ліку і тэорыя Дэмакрыта, распаўсюджвання і развіцця атрымаць не магло ў прынцыпе. І толькі ў XVIII стагоддзі навукоўцы зноў вяртаюцца да атамістычнай тэорыі. Да таго часу хімік А. Лавуазье, наш вялікі М. В. Ламаносаў і найталенавіты англійская фізік Д. Дальтона (аб якім мы пагаворым асобна), ўжо пераканаўча даказалі сваім калегам рэальнасць існавання атамаў. Варта падкрэсліць, што нават у асвечаным 18 стагоддзі доўгі час атамарнага тэорыя многімі выбітнымі розумамі таго часу сур'ёзна не разглядалася.
Як бы там ні было, але нават гэтыя вялікія навукоўцы яшчэ не вылучалі тэорый аб будынку самога атама, так як ён лічыўся адзінай і непадзельнай часцінкай, асновай усяго існага.
Да жаль, хімічныя досведы не маглі наглядна даказаць рэальнасць ператварэння атамаў адных рэчываў у іншыя. Але ўсё ж асноўнай навукай у вывучэнні будовы атамаў стала менавіта хімія. Атамы і малекулы доўгі час вывучаліся адным геніяльным рускім навукоўцам, без якога нельга ўявіць сабе сучасную навуку.
Вучэнне Д. І. Мендзялеева
 Велізарную ролю ў станаўленні атамарнага вучэнні адыграў Д. І. Мендзялееў, які яшчэ ў 1869 годзе стварыў сваю геніяльную перыядычную сістэму. Упершыню навуковаму супольнасці была прадстаўлена тэорыя, якая не толькі не адпрэчвала, але і разумна дапаўняла ўсё здагадкі матэрыялістаў. Ужо ў 19 стагоддзі навукоўцы змаглі даказаць існаванне электронаў. Усе гэтыя высновы прымусілі лепшыя розумы 20-га стагоддзя сур'ёзна вывучыць атам. У хіміі гэта час таксама было адзначана мноствам адкрыццяў.
Велізарную ролю ў станаўленні атамарнага вучэнні адыграў Д. І. Мендзялееў, які яшчэ ў 1869 годзе стварыў сваю геніяльную перыядычную сістэму. Упершыню навуковаму супольнасці была прадстаўлена тэорыя, якая не толькі не адпрэчвала, але і разумна дапаўняла ўсё здагадкі матэрыялістаў. Ужо ў 19 стагоддзі навукоўцы змаглі даказаць існаванне электронаў. Усе гэтыя высновы прымусілі лепшыя розумы 20-га стагоддзя сур'ёзна вывучыць атам. У хіміі гэта час таксама было адзначана мноствам адкрыццяў.
Але вучэнне Мендзялеева каштоўна не толькі гэтым. Да гэтага часу застаецца незразумелым, як менавіта фармаваліся атамы розных хімічных элементаў. Але вялікі рускі вучоны змог пераканаўча даказаць, што усе яны, без выключэння, знаходзяцца ў блізкім сваяцтве адзін з адным.
Адкрыццё Дальтона
Але здолець інтэрпрэтаваць шматлікія разрозненыя дадзеныя змог толькі Джон Дальтона, імя якога навекі адлюстравана ў адкрытым ім самім законе. Звычайна вучоны даследаваў толькі паводзіны газаў, але круг інтарэсаў у яго быў нашмат шырэй. У 1808 годзе ён прыступіў да публікацыі сваёй новай фундаментальнай працы.
Менавіта Дальтона выказаў здагадку, што кожнаму хімічным элементу адпавядае пэўны атам. Але вучоны,як і Дэмакрыт за шмат стагоддзяў да яго, усё ж лічыў, што яны з'яўляюцца цалкам непадзельныя. У яго чарнавіках нямала схематичных малюнкаў, на якіх атамы прадстаўлены ў выглядзе простых шарыкаў. Гэтая ідэя, якая зарадзілася больш за 2500 гадоў таму, праіснавала ледзь не да нашага часу! Зрэшты, толькі параўнальна нядаўна было адкрыта сапраўды глыбокае будова атама. Хімія (9 клас у прыватнасці) нават сёння шмат у чым кіруецца тымі ідэямі, якія былі ўпершыню агучаныя ў 18 стагоддзі.
Эксперыментальныя пацверджання дзялімасці атамаў
Зрэшты, да канца 19 стагоддзя практычна ўсе навукоўцы лічылі, што атам - тая мяжа, за якім нічога няма. Яны думалі, што асновай усяго светабудовы з'яўляецца менавіта ён. Гэтаму спрыялі розныя эксперыменты: як ні круці, але змяняліся толькі малекулы, у той час як з самімі атамамі рэчываў не адбывалася роўным лікам нічога, чаго б не змагла растлумачыць найпростая хімія. Будова атама вугляроду, да прыкладу, застаецца цалкам нязменным нават у розных аллотропных станах.
Словам, доўгі час не было роўным лікам ніякіх эксперыментальных дадзеных, якія хоць бы ўскосна пацвярджалі падазрэнні некаторых навукоўцаў аб тым, што маюцца якія-то больш фундаментальныя часціцы. Толькі ў 19 стагоддзі (не ў апошнюю чаргу дзякуючы доследам мужа і жонкі Кюры) было даказана, што ў пэўных умовах атамы адных элементаў могуць ператварацца ў іншыя. Гэтыя адкрыцця ляглі ў аснову сучасных уяўленняў аб навакольным нас свеце.
Разынкі і пудынгі
У 1897 годзе Дж. Томсанам, ангельскай фізікам, было ўстаноўлена, што ў любым атаме маецца нейкае колькасць адмоўна зараджаных часціц, якія ён жа назваў «электронамі». Ужо ў 1904 годзе вучоны стварыў першую атомарную мадэль, якая больш вядомая пад пазначэннем «пудынг з разынкамі». Назва цалкам дакладна адлюстроўвае сутнасць. Мяркуючы па тэорыі Томсана, атам у хіміі – гэта нейкі «посуд» з раўнамерна размеркаваным у ім зарадам і электронамі.
Заўважым, што падобная мадэль мела хаджэнне нават у 20-м стагоддзі. Пасля аказалася, што яна была зусім няслушнай. Але ўсё ж гэта была першая ўсвядомленая спроба чалавека (прычым на навуковай аснове) узнавіць навакольны яго мікрасвет, прапанаваўшы мадэль атама, дастаткова простую і навочную.
Досведы Кюры
Прынята лічыць, што муж і жонка П'ер і Марыя Кюры паклалі пачатак атамнай фізіцы. Вядома ж, ўклад гэтых геніяльных людзей, фактычна пожертвовавших сваім здароўем і жыццём, нельга недаацаніць, але іх досведы мелі і куды больш фундаментальнае значэнне. Практычна адначасова з Резерфордом яны даказалі, што атам – значна больш складаная і разнародная структура. Само з'ява радыеактыўнасці, якое яны даследавалі, менавіта пра гэта і казала.
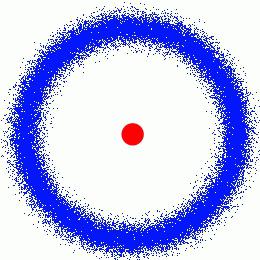 Ужо у пачатку 1898 года Марыя публікуе першую артыкул, прысвечаную радыяцыі. Неўзабаве Марыя і П'ер Кюры даказалі, што ў сумесі хлорыстых злучэнняў ўрану і радыя пачынаюць з'яўляцца іншыя рэчывы, у існаванні якіх сумнявалася афіцыйная хімія. Будова атама з тых часоў пачалі даследаваць ўшчыльную.
Ужо у пачатку 1898 года Марыя публікуе першую артыкул, прысвечаную радыяцыі. Неўзабаве Марыя і П'ер Кюры даказалі, што ў сумесі хлорыстых злучэнняў ўрану і радыя пачынаюць з'яўляцца іншыя рэчывы, у існаванні якіх сумнявалася афіцыйная хімія. Будова атама з тых часоў пачалі даследаваць ўшчыльную.
«Планетарны» падыход
Нарэшце Радэрфорд вырашыў вырабіць бамбаванне атамаў цяжкіх металаў α-часціцамі (цалкам іянізаванай гелій). Вучоны адразу ж выказаў здагадку, што лёгкія электроны ніяк не змогуць памяняць траекторыю руху часціц. Адпаведна, рассейванне могуць выклікаць толькі якія-то больш цяжкія элементы, якія могуць утрымлівацца ў ядры атама. Адразу заўважым, што першапачаткова Радэрфорд ніяк не прэтэндаваў на змяненне тэорыі «пудынгу». Гэтая мадэль атама лічылася бездакорнай.
А таму вынік, пры якім амаль усе часціцы без праблем праходзілі праз тонкі пласт срэбра, яго не здзівіў. Вось толькі неўзабаве высветлілася, што некаторыя атамы гелія адхіляліся адразу на 30°. Гэта было зусім не тое, пра што казала ў той час хімія. Склад атама па Томсан меркаваў раўнамернае размеркаванне электронаў. Але гэтага відавочна супярэчылі назіраныя з'явы.
Надзвычай рэдка, але ўсё ж некаторыя часціцы ляцелі пад вуглом нават 180°. Радэрфорд быў у глыбокім здзіўленні. Бо гэта рэзка супярэчыла «пудингу», зарад у якім павінен быў быць (па тэорыі Томсана) размеркаваны раўнамерна. Такім чынам, нераўнамерна зараджаныя ўчасткі, якія маглі б адштурхоўваць іянізаванай гелій, павінны былі адсутнічаць.
Да якіх высноваў прыйшоў Радэрфорд?
Гэтыя абставіны і падштурхнулі на думку вучонага, што атам практычна пусты і толькі ў цэнтры засяроджана якое-то адукацыю з станоўчым зарадам - ядро. Так і ўзнікла планетарная мадэль атама, пастулаты якой наступныя:
- Як мы ўжо казалі, у цэнтральнай частцы размешчана ядро, прычым яго аб'ём (па адносінах да памеры самога атама) нікчэмна малы.
- Практычна ўся атамарнага маса, а таксама ўвесь станоўчы зарад знаходзяцца менавіта ў ядры.
- Вакол яго круцяцца электроны. Важна, што іх колькасць роўна значэнню станоўчага зарада.
Парадоксы тэорыі
 Усё было б добра, але дадзеная мадэль атама ніяк не тлумачыць іх неверагодную ўстойлівасць. Варта памятаць, што электроны рухаюцца па сваіх арбітах з велізарным паскарэннем. Па ўсіх законах электрадынамікі такі аб'ект з часам павінен страціць свой зарад. Калі прымаць пад увагу пастулаты Ньютана і Максвелла, тоэлектроны наогул павінны сыпацца на ядро, нібы град на зямлю.
Усё было б добра, але дадзеная мадэль атама ніяк не тлумачыць іх неверагодную ўстойлівасць. Варта памятаць, што электроны рухаюцца па сваіх арбітах з велізарным паскарэннем. Па ўсіх законах электрадынамікі такі аб'ект з часам павінен страціць свой зарад. Калі прымаць пад увагу пастулаты Ньютана і Максвелла, тоэлектроны наогул павінны сыпацца на ядро, нібы град на зямлю.
Вядома, нічога такога ў рэальнасці не адбываецца. Любы атам не толькі цалкам устойлівы, але і можа існаваць цалкам неабмежаваны час, прычым ніякага выпраменьвання ад яго ісці не будзе. Такое неадпаведнасць тлумачыцца тым, што да микромиру мы спрабуем прымяняць законы, якія сапраўдныя толькі ў дачыненні да класічнай механікі. Яны ж, як аказалася, да з'яў атамарнага маштабу зусім непрыдатныя. А таму будова атама (хімія, 11 клас) аўтары падручнікаў імкнуцца растлумачыць як мага больш простымі словамі.
Вучэнне Бору
Дацкім фізікам Нільсэн Борам было даказана, што на мікрасвет нельга распаўсюджваць тыя ж законы, палажэнні якіх справядлівыя для макраскапічным аб'ектаў. Менавіта яму належыць ідэя аб тым, што мікрасвет «кіруецца» выключна квантавымі законамі. Вядома, тады не існавала самой квантавай тэорыі, але Бор фактычна стаў яе пачынальнікам, выказаўшы свае думкі ў выглядзе трох пастулатаў, якія «ратавалі» атам, немінуча б загінуў, калі б ён «жыў» паводле тэорыі Рэзерфорда. Менавіта гэтая тэорыя датчаніна легла ў аснову ўсёй квантавай механікі.
Пастулаты Бора
- Першы з іх абвяшчае: любая атамная сістэма можа знаходзіцца толькі ў адмысловых атамных станах, прычым для кожнага з іх характэрна пэўнае значэнне энергіі (Е). Калі стан атама стацыянарнае (спакойны), то выпраменьваць ён не можа.
- Другі пастулат кажа аб тым, што выпраменьванне светлавой энергіі адбываецца толькі ў выпадку пераходу з стану з большай энергіяй у больш умеранае. Адпаведна, якая выдаткоўваецца энергія роўная розніцы значэнняў паміж двума стацыянарнымі станамі.
Мадэль атама Нільса Бора
Гэтую полуклассическую тэорыю навуковец прапанаваў у 1913 годзе. Характэрна, што ў яе аснову ён паклаў планетарную мадэль Рэзерфорда, які незадоўга да яго апісаў атам рэчыва. Мы ўжо казалі, што класічная механіка супярэчыла выкладкі Рэзерфорда: зыходзячы з яе, меркавалася, што з часам электрон павінен быў абавязкова зваліцца на паверхню атама.
Каб «абыйсці» гэта супярэчнасць, вучоны ўвёў спецыяльнае дапушчэнне. Яго сутнасць заключалася ў тым, што выпраменьваць энергію (што і павінна было прывесці да іх падзення) электроны могуць, толькі рухаючыся па нейкім вызначаным арбітах. Пры руху іх па іншых траекторыях нібыта хімічныя атамы заставаліся ў пасіўным стане. Паводле тэорыі Бора такімі арбіты з'яўляліся тыя, колькасны момант руху па якім быў роўны пастаянным Планка.
Квантавая тэорыя будовы атама
 Як мы ўжо казалі, на сённяшні дзень у хаду квантавая тэорыя будовы атама. Хімія апошніх гадоў кіруецца выключна ёю. У яе аснове ляжаць чатыры асноватворных аксіёмы.
Як мы ўжо казалі, на сённяшні дзень у хаду квантавая тэорыя будовы атама. Хімія апошніх гадоў кіруецца выключна ёю. У яе аснове ляжаць чатыры асноватворных аксіёмы.
1. Па-першае, дваістасць (карпускулярна-хвалевая прырода) самага электрона. Прасцей кажучы, паводзіць сябе гэтая часціца і як матэрыяльны аб'ект (корпускула), і як хваля. Як часціца ён мае пэўны зарад і масу. Здольнасць жа да дыфракцыі радніць электроны з класічнымі хвалямі. Даўжыня гэтай самай хвалі (λ) і хуткасць часціцы (v) могуць быць звязаны адзін з адным спецыяльным суадносінамі дэ Бройлем: λ = h / mv. Як можна здагадацца, m – маса самага электрона.
2. Каардынату і хуткасць часціцы замерыць з абсалютнай дакладнасцю цалкам немагчыма. Чым дакладней вызначаецца каардыната, тым вышэй нявызначанасць у хуткасці. Як, зрэшты, і наадварот. Гэта з'ява атрымала назву нявызначанасці Гейзенберга, якое можа быць выказана ў выглядзе наступнага суадносін: ∆x∙m∙∆v > ћ/2. Дэльта Х (∆x) выказвае нявызначанасць становішча каардынаты ў прасторы. Адпаведна, дэльта V (∆v) адлюстроўвае хуткасныя хібнасці.
3. Насуперак усім раней распаўсюджаным меркаванням, электроны не праходзяць па строга вызначаным арбітах, як цягнік па рэйках. Квантавая тэорыя абвяшчае, што электрон можа знаходзіцца ў любой кропцы прасторы, але верагоднасць гэтага розная для кожнага адрэзка.
Тая частка прасторы вакол непасрэдна атамнага ядра, у якой гэтая верагоднасць максімальная, называецца орбиталью. Сучасная хімія будова электронных абалонак атамаў вывучае менавіта з гэтай кропкі гледжання. Вядома, у школах вучаць правільнаму размеркаванні электронаў па ўзроўнях, але, па ўсёй бачнасці, у рэальнасці яны разыходзяцца зусім інакш.
4. Ядро атама складаецца з нуклонов (пратонаў і нейтронаў). Парадкавы нумар элемента ў перыядычнай сістэме паказвае на колькасць пратонаў у яго ядры, а сума пратонаў і нейтронаў роўная атамарна масе. Вось як тлумачыць будова ядра атама хімія сучаснасці.
Заснавальнікі квантавай механікі
 Адзначым тых навукоўцаў, якія ўнеслі найбольшы ўклад у развіццё такой важнай галіны: французскі фізік Л. дэ Бройль, немец В. Гейзенберг, аўстрыец. Э. Шредингер, ангелец. П. Дирак. Усе гэтыя людзі пасля былі ўдастоены Нобелеўскай прэміі.
Адзначым тых навукоўцаў, якія ўнеслі найбольшы ўклад у развіццё такой важнай галіны: французскі фізік Л. дэ Бройль, немец В. Гейзенберг, аўстрыец. Э. Шредингер, ангелец. П. Дирак. Усе гэтыя людзі пасля былі ўдастоены Нобелеўскай прэміі.
Як жа далёка ў гэтым плане пайшла хімія? Будова атама большасць хімікаў тых гадоў лічылі досыць простым: многія толькі да 1947 годзе канчаткова прызналі рэальнасць існавання элементарных часціц.
Некаторыя высновы
Наогул, пры стварэнні квантавай тэорыі не абышлося без матэматыкаў, так як усе гэтыя працэсы можна разлічыць толькі з выкарыстаннемскладаных вылічэнняў. Але самая галоўная цяжкасць заключаецца зусім не ў гэтым. Тыя працэсы, якія апісваюцца дадзенай тэорыяй, недаступныя не толькі нашым органам пачуццяў, нягледзячы на ўсю сучасную навуковую тэхніку, але і ўяўленню.
Ні адзін чалавек нават прыблізна не можа ўявіць сабе працэсы ў мікрасвеце, так як яны зусім не падобныя на ўсе тыя з'явы, якія мы назіраем у макрасвет. Удумайцеся толькі: апошнія адкрыцця даюць падставу меркаваць, што кварк, нейтрына і іншыя фундаментальныя часціцы існуюць у девятимерном (!) вымярэнні. Як чалавек, які жыве ў трохмернай прасторы, можа нават прыблізна апісаць іх паводзіны?
У сапраўдны момант нам застаецца толькі спадзявацца на матэматыку і моц сучасных кампутараў, якія, можа быць, будуць выкарыстаны для мадэлявання мікрасвету. Адчувальна дапамагае і хімія: будова атама, напэўна, будзе перагледжана, пасля таго як нядаўна навукоўцы, якія працуюць у гэтай галіне, паведамілі аб адкрыцці новага тыпу хімічнай сувязі.
Сучаснае ўяўленне аб будове атама
Калі вы ўважліва прачыталі ўсё вышэйпададзенае, то, напэўна, і самі зможаце сказаць, якое сённяшняе ўяўленне аб будове атамаў рэчываў. Але ўсё ж мы растлумачым: гэта некалькі перайначаны тэорыя Рэзерфорда, дапоўненая неацэннымі пастулатамі Нільса Бора. Прасцей кажучы, сёння лічыцца, што электроны рухаюцца па хаатычным, размытым траекторыях каля ядра, якое складаецца з нейтронаў і пратонаў. Тая частка прасторы вакол яго, у якой з'яўленне электрона найбольш верагодна, называецца орбиталью.
Пакуль не ўяўляецца магчымым дакладна сказаць, як будуць мяняцца нашы ўяўленні аб будове атама ў далейшым. Штодня навукоўцы працуюць над пранікненнем у таямніцы мікрасвету: БАК (Вялікі андронный коллайдер), Нобелеўскія прэміі ў галіне фізікі – усё гэта з'яўляецца вынікам дадзеных пошукаў.
Але нават цяпер мы не ўяўляем і прыблізнай карціны таго, што яшчэ хаваюць атамы. Зразумела толькі, што сам атам у маштабах мікрасвету – велізарны шматкватэрны дом, у якім намі абследаваны хіба што першы паверх, ды і тое не цалкам. Практычна штогод з'яўляюцца паведамленні аб магчымасці адкрыцця ўсё новых і новых элементарных часціц. Калі працэс даследавання атамаў будзе цалкам скончаны, сёння прагназаваць не возьмецца ніхто.
 Дастаткова сказаць, што нашы ўяўленні пра іх пачалі мяняцца толькі з 1947 года, калі былі адкрыты так званыя V-часціцы. Да гэтага людзі толькі трохі паглыбілі тэорыі, на якіх з 19 стагоддзя грунтавалася хімія. Будова атама – займальная загадка, разгадваннем якой занятыя лепшыя розумы чалавецтва.
Дастаткова сказаць, што нашы ўяўленні пра іх пачалі мяняцца толькі з 1947 года, калі былі адкрыты так званыя V-часціцы. Да гэтага людзі толькі трохі паглыбілі тэорыі, на якіх з 19 стагоддзя грунтавалася хімія. Будова атама – займальная загадка, разгадваннем якой занятыя лепшыя розумы чалавецтва.
Article in other languages:
KK: https://tostpost.com/kk/b-l-m/33409-atom-himiya---b-l-model-atom-fizikasy-atom-rylysy.html
PL: https://tostpost.com/pl/edukacja/34457-atom-w-chemii---to-model-atomu-budowa-atomu.html
TR: https://tostpost.com/tr/e-itim/29835-atom-kimya-atom-modeli-atomun-yap-s.html
UK: https://tostpost.com/uk/osv-ta/33603-atom-u-h-m---ce-model-atoma-budova-atoma.html

Alin Trodden - аўтар артыкула, рэдактар
"Прывітанне, Я Алін Тродден. Я пішу тэксты, чытаю кнігі і шукаю ўражанні. І я нядрэнна ўмею распавядаць вам пра гэта. Я заўсёды рады ўдзельнічаць у цікавых праектах."
Навіны
Куды можа прывесці бесперапыннае адукацыю
З нараджэння да смерці чалавеку даводзіцца пастаянна вучыцца для таго, каб выжыць, каб прыстасавацца да зменлівай рэчаіснасці, каб знайсці і спазнаць самога сябе і разумна пражыць сваё жыццё. Канцэпцыя бесперапыннага адукацыі, нав...
Ўводны абарот. Уступныя словы, словазлучэнні і прапановы. Пастаноўка знакаў прыпынку
У сваёй прамове людзі даволі часта выкарыстоўваюць уступныя канструкцыі, каб паказаць сваё стаўленне да таго, аб чым менавіта яны распавядаюць. Пры напісанні ўводны абарот абавязкова вылучаецца коскамі, а ў вуснай гаворкі такі аба...
На якой рацэ стаіць Казань. Прыродныя славутасці Казані
Казань – сталіца Татарстана. Горад валодае тысячагадовай гісторыяй, самабытнай культурай, развітой эканомікай, з'яўляецца навуковым цэнтрам рэспублікі. На яго тэрыторыі размешчаны буйны порт. На якой рацэ стаіць Казань &ndas...
Антонімы – гэта проціпастаўленне адзін аднаму па сэнсу, але якія належаць да адной і той жа часціны мовы словы. Яны маюць рознае напісанне і гучанне. Вызначыць значэнне аднаго антонима вельмі проста праз іншы, досыць надаць ...
Кім быў першы вынаходнік радыё?
А. С. Папоў - вынаходнік радыё, якім па праву можа ганарыцца наша краіна. Ён першым пачаў вывучаць электрамагнітныя хвалі, і нават быў выкладчыкам адпаведных курсаў для афіцэраў. Менавіта Папоў знайшоў практычнае прымяненне электр...
"СМІ": лексічнае значэнне слова, сінонімы і тлумачэнне
Складанасць вызначэння лексічнага значэння слова «СМІ» у тым, што слоўнік дае толькі расшыфроўку абрэвіятуры. Таму больш поўнае разуменне тэрміна прыйдзецца сфармуляваць самім, таксама разгледзім сінонімы і тлумачэнне ...





















Заўвага (0)
Гэтая артыкул не мае каментароў, будзьце першым!