Now - 13:42:00
Ідеальний газ. Рівняння стану ідеального газу. Изопроцессы.
Ідеальний газ, рівняння стану ідеального газу, його температура і тиск, об'єм… список параметрів і ухвал, якими оперують у відповідному розділі фізики, можна продовжувати досить довго. Сьогодні ми поговоримо саме на цю тему.
Що розглядається в молекулярній фізиці?

Основним об'єктом, який розглядається в цьому розділі, є ідеальний газ. Рівняння стану ідеального газу було отримано з урахуванням нормальних умов навколишнього середовища, та про це ми поговоримо трохи пізніше. Зараз давайте підійдемо до цієї “проблеми” здалеку.
Припустимо, у нас є деяка маса газу. Її стан можна визначити за допомогою трьох параметрів термодинамічного характеру. Це, звичайно ж, тиск, об'єм і температура. Рівняння стану системи в цьому випадку буде формула зв'язку між відповідними параметрами. Вона виглядає таким чином: F (p, V, T) = 0.
Ось тут ми вперше потихеньку підбираємося до появи такого поняття, як ідеальний газ. Їм називається газ, в якому взаємодії між молекулами пренебрежимо малі. Взагалі в природі такого не існує. Однак будь-сильно розріджений газ близький до нього. Від ідеального мало чим відрізняються азот, кисень повітря, що знаходяться в нормальних умовах. Щоб записати рівняння стану ідеального газу, ми можемо використовувати об'єднаний газовий закон. Одержимо: pV/T = const.
Пов'язане поняття № 1: закон Авогадро
Він може розповісти нам про те, що якщо ми візьмемо однакову кількість молей абсолютно будь-якого випадкового газу і поставимо їх в однакові умови, серед яких температура і тиск, то гази займуть однаковий обсяг. Зокрема, досвід проводився при нормальних умовах. Це означає, що температура дорівнювала 273,15 Кельвинам, тиск - одній атмосфері (760 міліметрів ртутного стовпа або ж 101325 Паскаль). При таких параметрах газ зайняв обсяг дорівнює 22,4 літра. Отже, ми можемо говорити про те, що для одного моля будь-якого газу співвідношення числових параметрів буде величиною постійною. Саме тому було прийнято рішення цієї цифри дати позначення буквою R і назвати її універсальної газової сталої. Таким чином, вона дорівнює 8,31. Розмірність Дж/моль*К.
Більше:
Перший штучний супутник Землі є одним з найбільших досягнень науки ХХ століття. Тим не менш, як це ні парадоксально, цьому великому науковому і технічному досягненню значною мірою сприяла холодна війна між двома наддержавами: США і Радянським Союзом....
Що таке соціалізація, і як вона змінює людину
Спробуємо розібратися, що таке соціалізація, в чому її сутність і особливість. Адже для кожної особистості входження у суспільство і засвоєння його основних норм є фундаментом до подальшої безпроблемною і успішного життя і діяльності. Отже, що таке с...
Принц Чарльз – головний спадкоємець британського престолу
Згідно із законом королівства Великобританія, спадкоємець британського престолу - це старший закононароджена син чинного монарха або ж попереднього претендента на престол. Однак якщо у царюючого особи немає дитини чоловічої статі, то право спадкуванн...
Ідеальний газ. Рівняння стану ідеального газу і маніпуляції з ним
Давайте спробуємо переписати формулу. Для цього запишемо його в такому вигляді: pV = RT. Далі здійснимо нехитра дія, помножимо обидві частини рівняння на довільну кількість молей. Отримаємо pVu = uRT. Приймемо до уваги той факт, що твір молярного об'єму на кількість речовини є просто обсяг. Але ж кількість молей одночасно буде дорівнювати приватному маси та молярної маси. Саме так виглядає рівняння Менделєєва-Клапейрона. Воно дає чітке поняття про те, яку систему утворює ідеальний газ. Рівняння стану ідеального газу прийме вигляд: pV = mRT/M.
Виведемо формулу для тиску
Давайте проведемо ще деякі маніпуляції з отриманими виразами. Для цього праву частину рівняння Менделєєва-Клапейрона помножимо і розділимо на число Авогадро. Тепер уважно дивимося на добуток кількості речовини на число Авогадро. Це є не що інше, як загальне число молекул в газі. Але в той же час ставлення універсальної газової сталої до числа Авогадро буде дорівнює постійної Больцмана. Отже, формули для тиску можна записати таким чином: p = NkT/V або p = nkT. Тут позначення n це концентрація частинок.
Процеси ідеального газу
В молекулярній фізиці існує таке поняття, як изопроцессы. Це термодинамічні процеси, які мають місце в системі при одному з постійних параметрів. При цьому маса речовини також повинна залишатися постійною. Давайте розглянемо їх більш конкретно. Отже, закони ідеального газу.
Постійним залишається тиск
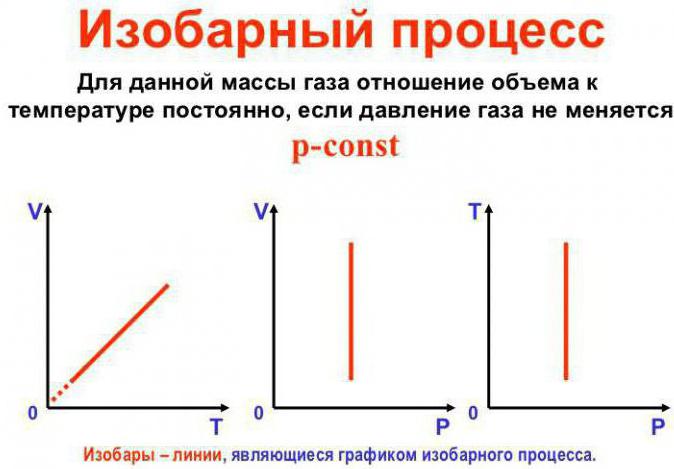
Це закон Гей-Люссака. Виглядає він так: V/T = const. Його можна переписати і по-іншому: V = Vo (1+at). Тут a дорівнює 1/273,15 До^-1 і носить назву "коефіцієнт об'ємного розширення". Ми можемо підставити температуру як за шкалою Цельсія, так і за шкалою Кельвіна. В останньому випадку отримаємо формулу V = Voat.
Постійним залишається обсяг

Це другий закон Гей-Люссака, більш часто називають законом Шарля. Виглядає він так: p/T = const. Є й інша формулювання: p = po (1 + at). Перетворення можуть бути проведені у відповідності з попереднім прикладом. Як можна бачити, закони ідеального газу іноді бувають досить схожими один на одного.
Постійним залишається температура

Якщо температура ідеального газу залишається величиною постійною, то ми можемо отримати закон Бойля-Маріотта. Він може бути записаний таким чином: pV = const.
Пов'язане поняття № 2: парціальний тиск
Припустимо, у нас є посудину з газами. Це буде суміш. Система знаходиться в стані теплової рівноваги, а самі гази між собою не реагують. Тут N буде позначати загальна кількість молекул. N1, N2 і так далі, відповідно, кількість молекул у кожному з компонентів наявної суміші. Візьмемо формулу тиску p = nkT = NkT/V. Її можна розкрити для конкретного випадку. Для двокомпонентної суміші формула прийме вигляд: p = (N1 + N2) kT/V. Але тодівийде, що загальний тиск буде підсумовуватися з приватних тисків кожної суміші. А отже, воно буде мати вигляд p1 + p2 і так далі. Це і будуть парціальні тиску.
Для чого це потрібно?
Отримана нами формула вказує на те, що тиск в системі виявляється з боку кожної групи молекул. Воно, до речі, не залежить від інших. Цим скористався Дальтон при формулюванні закону, названого згодом на його честь: в суміші, де гази не реагують між собою хімічно, загальний тиск буде дорівнює сумі парціальних тисків.
Article in other languages:
KK: https://tostpost.com/kk/b-l-m/14088-idealdy-gaz-ideal-gaz-k-y-n-te-deu-izoprocester.html
TR: https://tostpost.com/tr/e-itim/14090-deal-gaz-denklemi-ideal-gaz-izoprocessy.html

Alin Trodden - автор статті, редактор
"Привіт, Я Алін Тродден. Я пишу тексти, читаю книги і шукаю враження. І я непогано вмію розповідати вам про це. Я завжди радий брати участь у цікавих проектах."
Новини
Наголос у слові "кошти". Правила наголосу
Мова людини - основа його репутації серед оточуючих. Важливо пам'ятати, що в цивілізованому суспільстві ніщо: ні виховання, ні оточення, ні культура, що панує навколо, - не виправдовує неписьменною мови. Хоча часом слух можуть різ...
Шкала Кардашева: цивілізація другого типу
Людина завжди мріяв дізнатися, чи один він у Всесвіті чи десь існують інші розумні істоти, що досягли найвищого рівня розвитку. А яким він може бути, цей рівень? Що брати за ступінь розвиненості цивілізації? Вже багато років тому ...
У даній статті мова піде про незамінного ферменті, що знаходиться в шлунку у кожного ссавця, включаючи людину. Будуть розглянуті загальні відомості про ферменті пепсине, інформація про його изомерах і речовини роль в процесах трав...
Як сформулювати проблему тексту?
В останньому завданні ЄДІ з російської мови від учня потрібно прочитати текст і відшукати наявну проблему. Таких в завданні є три, іноді більше. Проблеми з їх визначенням виникають нечасто. Однак слід детально розглянути цей проце...
Нюанс - це тонкість. Значення, правопис, тлумачення
В житті багато тонкощів. Нехай ця проста думка стане прологом до нашої розмови. А говоримо ми сьогодні про нюанси – це, як відомо, різні деталі.Тлумачний словник – річ абсолютно прекрасна і незамінна, особливо коли пот...
Південно-Східний фронт (Громадянська війна): склад, бойові дії
Що собою представляв Південно-Західний фронт Червоної армії? Які бойові дії відбувалися на цьому напрямку? Відповіді на ці та інші питання ви знайдете в статті. Відомо, що Південно-Західний фронт – це стратегічний оперативни...






















Примітка (0)
Ця стаття не має коментарів, будьте першим!