Миш'якова кислота: хімічні властивості, формула. Високонебезпечні речовини
Вплив різних хімічних речовин на організм людини неоднозначно. Більшість відомих нам сполук або є нейтральними, або грають позитивну роль у життєдіяльності людини. Але є група речовин, що становлять серйозну загрозу для здоров'я. Вони розділені на кілька класів. Розглянута в даній статті миш'якова кислота – одне з таких токсичних хімічних сполук. Відповідно до прийнятої в даний час класифікації, вона входить у другий клас підвищеної небезпеки, поряд з хлороформом, сполуками свинцю та літію. Вивчимо властивості миш'яковистої кислоти більш докладно.
Будова молекули і агрегатний стан речовини
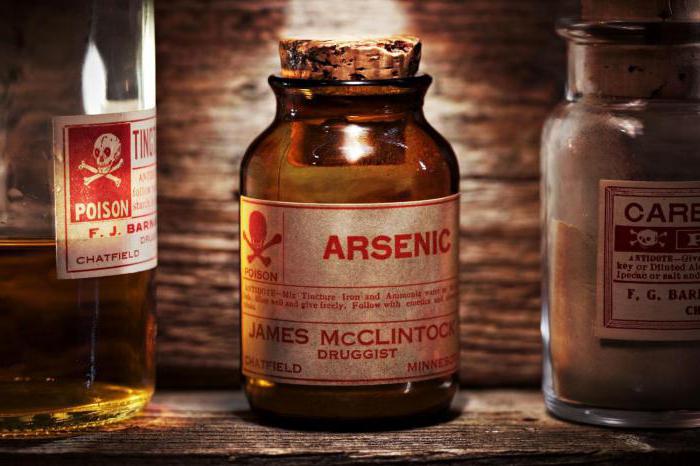
Це з'єднання при звичайних умовах має кристалічну структуру. Будучи трехосновной, миш'якова кислота, формула якої H3AsO4, має як середні, так і кислі солі. Наприклад, гидроарсенат калію – K2HAsO4, дигидроарсенат натрію – NaH2AsO4, арсенат літію – Li3AsO4. Прокаливая миш'якових кислоту, отримують гемипентоксид миш'яку, званий мышьяковым ангідридом. Його білі прозорі кристали утворюють склоподібну масу, яка розчиняється погано у воді.
Дисоціація
H3AsO4, поряд з мурашиною кислотою і гідроксидом свинцю, є помірно слабким електролітом. Так, в таблиці іонізації найважливіших кислот ортомышьяковая кислота має три константи дисоціації: 5,6 х 10-3, 1,5 х 10-7 3, 89 х 10-12. Ці показники кількісно характеризують силу кислоти. Згідно з константами дисоціації, в ряду неорганічних кислот H3AsO4 займає положення між хромової і сурм'яної кислотами. Російські хіміки-експериментатори А. Л. і В. Л. Агафоновы сформулювали математичне вираз, в якому вивели залежність першої та другої константи дисоціації миш'яковистої кислоти від температури в інтервалі від 0°С до 50°C
Більше:
Перший штучний супутник Землі є одним з найбільших досягнень науки ХХ століття. Тим не менш, як це ні парадоксально, цьому великому науковому і технічному досягненню значною мірою сприяла холодна війна між двома наддержавами: США і Радянським Союзом....
Що таке соціалізація, і як вона змінює людину
Спробуємо розібратися, що таке соціалізація, в чому її сутність і особливість. Адже для кожної особистості входження у суспільство і засвоєння його основних норм є фундаментом до подальшої безпроблемною і успішного життя і діяльності. Отже, що таке с...
Принц Чарльз – головний спадкоємець британського престолу
Згідно із законом королівства Великобританія, спадкоємець британського престолу - це старший закононароджена син чинного монарха або ж попереднього претендента на престол. Однак якщо у царюючого особи немає дитини чоловічої статі, то право спадкуванн...
Особливості хімічних властивостей
Ступінь окислення атома миш'яку, що входить до складу молекули кислоти, дорівнює +5. Це говорить про той факт, що саме з'єднання в хімічні реакції з іншими речовинами виявляє окисні властивості. Так, при її взаємодії з иодидом калію, виступаючим в якості відновника, в кислому середовищі серед продуктів реакції ми виявимо миш'яковисту кислоту H3AsO3. Нагадаємо, що миш'якова кислота, формула якої H3AsO4, є трехосновной, а значить, в реакціях з лугами або нерозчинними підставами вона може давати три типи солей: середні, гідро - і дигидроарсенаты. Якісною реакцією на іон AsO43- в аналітичній хімії служить взаємодія самої миш'яковистої кислоти або її солей з розчинними солями срібла, наприклад, з нітратом. В результаті спостерігаємо випадання осаду Ag3AsO4 кавового кольору.
Йодометричний метод визначення миш'яковистої кислоти
В аналітичній хімії важливим завданням є виявлення хімічних сполук у досліджуваних розчинах. Миш'якова кислота, хімічні властивості якої ми розглядали раніше, може бути виявлена микрометодом йодометрии. До 1 мл її розчину доливають такий же обсяг 4н. розчину соляної кислоти і 1 мл 4% розчину йодиду калію. Утворюється сесквиоксид миш'яку As2O3, маса якого при строгому дотриманні кількісних обсягів реагентів завжди однакова і дорівнює 0,5746 мг.

Окислювальна здатність миш'яковистої кислоти
Як відомо, H3AsO4, як і ортофосфорна кислота, є електролітом середньої сили. Її білі прозорі кристали, що розпливаються на повітрі і мають склад 2H3AsO4 х H2O. Її солі, які утворені лужними металами (як середні, так і кислі), у водних розчинах мають рН більше 7. Арсенати літію, калію, натрію та амонію добре розчинні у воді, а інші середні солі в ній не розчиняються. Миш'якова кислота – хороший окислювач. В окисно-відновних реакціях вона відновлюється до миш'яковистої кислоти або арсина.
H3AsO4 + 2e + 2H+ = H3AsO3 + H2O
H3AsO4 + 8e + 8H+ = AsH3 + 4H2O
Крім того, миш'якова кислота легко окислює різні метали, сульфитную і йодидную кислоти, а також сірководень.

Отримання миш'яковистої кислоти
В лабораторних умовах H3AsO4 може бути отримана реакцією сесквіоксіда миш'яку нітратній кислотою при нагріванні. У продуктах виявляється оксид тривалентного азоту і H3AsO4. Ще один спосіб одержання – це розчинення у воді оксиду миш'яку. Часто для її одержання застосовують одночасне окислення і гідролізу триалкиларсенитов підігрітим до 50° З розчином пероксиду водню. Одночасно з реакційної суміші відводять воду і спирт. Потім розчин упарюють і одержують миш'якових кислоту особливої чистоти. У природі сировиною для отримання миш'яковистої кислоти служать мінерали: арсенолит і арсенопирит, поклади яких багаті Челябінська і Читинська області Російської Федерації.
Застосування H3AsO4
Враховуючи той факт, що ортомышьяковая кислота є одним з найсильніших отрут. Її застосування в промисловості та побуті обмежена. Більш поширені солі – арсенати, чия токсичність значно менше, ніж усамої H3AsO4. Так, в деревообробній промисловості разом із сірчанокислим цинком і натрієвою сіллю пентахлорфенола, миш'якових кислоту застосовують для обробки деревини. Такий метод зводить до мінімуму втрати від руйнування целюлози грибковими інфекціями і личинками жуків-древоточцев. У медицині H3AsO4 застосовують у складі препарату «Атоксіл» для лікування протозойних інфекцій, таких як лямбліоз, балантидіаз, изоспороз.

Треба зазначити, що зараженість населення цими інфекціями в останній час різко зросла. Причин декілька – наприклад, зараження через продукти харчування, що містять спори найпростіших, через укуси комах або статевим шляхом. Миш'якова кислота використовується в якості вихідної речовини в процесах виробництва оптичних стекол, а також в електротехніці. Похідне H3AsO4 - її натрієву сіль, успішно застосовують в дерматології та фтизіатрії. Сполуки миш'яку використовуються у стоматології (миш'якова паста) як препарату, що використовується для зниження больової чутливості запаленого нерва при його видаленні із зубного каналу.
Дію кислоти на організм людини
Як вже було сказано раніше, H3AsO4 входить у другий клас підвищеної небезпеки – високо небезпечні речовини. Смертельною вважається дозування як самої кислоти та її солей в межах від 15 до 150 мг на кілограм маси тіла людини. Поряд з загальною отруйною ефектом, миш'якова кислота викликає некроз шкірних покривів і слизових оболонок внутрішніх органів: легенів, шлунка, кишечника.
В лабораторії при проведенні дослідів з арсенатами і H3AsO4 обов'язкове використання захисних рукавичок, а самі експерименти проводять під витяжкою. У разі інтоксикації на рівні клітини порушується її ферментативна система, так як відбувається інактивація ферментів. В організмі людини отруєння арсенатами призводить до парезів і навіть паралічів. В онкології при проведенні хіміотерапії при недотриманні режиму дозування препаратів реєструються випадки отруєння миарсенолом і новарсенолом. Перша допомога при отруєнні солями миш'яковистої кислоти полягає в негайному промиванні шлунка (наприклад, розчином унітіолу або препаратами діоксиду кремнію).

Щоб не допустити гострої ниркової недостатності, призначають процедуру гемодіалізу. В якості антидоту, крім 5% розчину унітіолу, можна використовувати антидот Стрижевського. До приїзду швидкої невідкладної допомоги в домашніх умовах для зниження рівня інтоксикації можна застосувати розчин лимонної кислоти, потім викликати блювання і промити шлунок. Всі лікувальні заходи необхідно проводити з дотриманням суворого постільного режиму під наглядом лікаря.
Article in other languages:

Alin Trodden - автор статті, редактор
"Привіт, Я Алін Тродден. Я пишу тексти, читаю книги і шукаю враження. І я непогано вмію розповідати вам про це. Я завжди радий брати участь у цікавих проектах."
Новини
Центральне співвідношення щелеп: визначення, методи
В ортопедичній стоматології використовується термін "оклюзія". Під ним розуміють змикання зубів. Існує 4 основних оклюзії і безліч проміжних. До перших відносять центральну, передня і 2 бокові. Центральна оклюзія відрізняється мак...
Яке було ставлення Блоку до революції 1917 року?
Ким тільки не був Олександр Олександрович Блок - поетом, письменником, публіцистом, драматургом, перекладачем, літературним критиком. Крім цього, А. А. Блок - один з класиків російської літератури двадцятого сторіччя. Немислимий р...
"Малий мала менше": значення фразеологізму
Фразеологізми - невід'ємні і яскраві звороти, ідіоми. Багато з них сформувалися в мові так давно, що застарілі слова в їх складі вже ускладнюють розуміння сенсу, хоча саме стійке словосполучення використовується і актуально. Напри...
Міжособистісні конфлікти: сутність, причини і типологія
Міжособистісні конфлікти являють собою конфлікти, які виникають у сфері людей у процесі їх психологічного і соціального взаємодії. Виходячи з такого розуміння, стає ясним, що в будь-якому суспільстві ймовірність їх появи досить ве...
Скільки букв в англійському алфавіті і як їх читати
Так важливо знати, скільки букв в англійському алфавіті? У цій статті ми дамо відповідь на це питання, а також висвітлимо інші важливі моменти.Цікаво знатиВ цій абетці 26 символів, а для порівняння: у російській - 33. На...
Де знаходиться Карфаген і який його слід в історії?
Стародавній Карфаген – одне з небагатьох держав, що кинули реальний виклик римським легіонам в третьому столітті до нашої ери. Перемога Риму призвела в підсумку їх цивілізацію до блискучого величі, а Карфаген був несправедли...





















Примітка (0)
Ця стаття не має коментарів, будьте першим!