Now - 03:56:25
Вуглець - це... Атом вуглецю. Маса вуглецю
Одним з найдивовижніших елементів, який здатний формувати величезну кількість різноманітних сполук органічної і неорганічної природи, є вуглець. Це настільки незвичайний за властивостями елемент, що ще Менделєєв пророкував йому велике майбутнє, кажучи про не розкритих поки особливості.
Пізніше це підтвердилося практично. Стало відомо, що він - основний біогенний елемент нашої планети, що входить до складу абсолютно всіх живих істот. Крім цього, здатний існувати в таких формах, які кардинально різняться за всіма параметрами, але при цьому складаються тільки з атомів вуглецю.
загалом, особливостей у цієї структури багато, саме з ними і постараємося розібратися в ході статті.
Вуглець: формула і становище в системі елементів
У періодичній системі елемент вуглець розташовується в IV (за новим зразком 14) групі, головній підгрупі. Його порядковий номер 6, а атомна вага 12,011. Позначення елемента знайомий Із говорить про його назву на латині - carboneum. Є кілька різних форм, у яких існує вуглець. Формула його тому буває різна і залежить від конкретної модифікації.
Проте для написання рівнянь реакцій позначення конкретне, звичайно, є. Загалом, коли йдеться про речовину в чистому вигляді, прийнята молекулярна формула вуглецю, без індексації.
Історія відкриття елементу
Сам по собі цей елемент відомий з самої давнини. Адже один з найголовніших мінералів у природі - це кам'яне вугілля. Тому для давніх греків, римлян та інших народностей секретом він не був.
Більше:
Перший штучний супутник Землі є одним з найбільших досягнень науки ХХ століття. Тим не менш, як це ні парадоксально, цьому великому науковому і технічному досягненню значною мірою сприяла холодна війна між двома наддержавами: США і Радянським Союзом....
Що таке соціалізація, і як вона змінює людину
Спробуємо розібратися, що таке соціалізація, в чому її сутність і особливість. Адже для кожної особистості входження у суспільство і засвоєння його основних норм є фундаментом до подальшої безпроблемною і успішного життя і діяльності. Отже, що таке с...
Принц Чарльз – головний спадкоємець британського престолу
Згідно із законом королівства Великобританія, спадкоємець британського престолу - це старший закононароджена син чинного монарха або ж попереднього претендента на престол. Однак якщо у царюючого особи немає дитини чоловічої статі, то право спадкуванн...
Крім цього різновиду, також використовували алмази і графіт. З останнім довгий час було багато заплутаних ситуацій, так як часто без аналізу складу за графіт приймали такі сполуки, як:
- сріблястий свинець;
- карбід заліза;
- сульфід молібдену.
Всі вони були пофарбовані в чорний колір і тому вважалися графітом. Пізніше це непорозуміння було роз'яснено, і дана форма вуглецю стала сама собою.
З 1725 року велике комерційне значення набувають алмази, а в 1970 освоєна технологія отримання їх штучним шляхом. З 1779 року, завдяки роботам Карла Шеєле, вивчаються хімічні властивості, які проявляє вуглець. Це послужило початком низки найважливіших відкриттів в області даного елемента і стало основою для з'ясування всіх його унікальних особливостей.

Ізотопи вуглецю і поширення в природі
Незважаючи на те що розглянутий елемент - один з найважливіших біогенних, його загальний вміст в масі земної кори становить 0,15 %. Так відбувається від того, що він піддається постійній циркуляції, природного кругообігу в природі.
У цілому можна назвати кілька сполук мінерального характеру, до складу яких входить вуглець. Це такі природні породи, як:
- доломіти та вапняки;
- антрацит;
- горючі сланці;
- природний газ;
- кам'яне вугілля;
- нафту;
- буре вугілля;
- торф;
- бітуми.
Крім цього, не слід забувати і про живих істот, які є просто сховищем вуглецевих сполук. Адже їм утворені білки, жири, вуглеводи, нуклеїнові кислоти, а значить найбільш життєво важливі структурні молекули. В цілому на перерахунок сухий маси тіла 70 кг 15 припадає на чистий елемент. І так у кожної людини, не кажучи вже про тварин, рослинах та інших істот.
Якщо ж розглянути склад повітря і води, тобто гідросферу в цілому і атмосферу, то тут присутня суміш вуглець-кисень, виражається формулою2. Діоксид або вуглекислий газ - один з основних газів, складових повітря. Саме в такому вигляді масова частка вуглецю становить 0,046%. Ще більше розчинено вуглекислого газу у водах Світового океану.
Атомна маса вуглецю як елемента становить 12,011. Відомо, що дана величина розраховується як середнє арифметичне між атомними вагами всіх існуючих в природі ізотопних різновидів, з урахуванням їх поширеності (в процентному співвідношенні). Так відбувається і у аналізованого речовини. Є три головних ізотопу, у вигляді яких знаходиться вуглець. Це:
- 12С - його масова частка в переважній більшості становить 98,93 %;
- 13С - 1,07 %;
- 14С - радіоактивний, період напіврозпаду 5700 років, стійкий бета-випромінювач.
У практиці визначення геохронологического віку зразків широко застосовується радіоактивний ізотоп 14С, який є індикатором, завдяки своєму тривалому періоду розпаду.

Алотропні модифікації елемента
Вуглець - це такий елемент, який у вигляді простої речовини існує в декількох формах. Тобто він здатний формувати саме велике з відомих на сьогодні число аллотропних модифікацій.
1. Кристалічні варіації - існують у вигляді міцних структур з правильними гратами атомного типу. До даної групи відносяться такі різновиди, как:
- алмазы;
- фуллерены;
- графиты;
- карбины;
- лонсдейлиты;
- вуглецеві волокна і трубки.
Всі вони розрізняються будовою кристалічної решітки, у вузлах яких - атом вуглецю. Звідси і абсолютно унікальні, не схожі властивості, як фізичні, так і хімічні.
2. Аморфні форми - їх утворює атом вуглецю, що входить до складудеяких природних сполук. Тобто це не чисті різновиди, а з домішками інших елементів в незначній кількості. В дану групу входять:
- активоване вугілля;
- кам'яний і деревний;
- сажа;
- вуглецева нанопена;
- антрацит;
- скловуглець;
- технічна різновид речовини.
Їх також об'єднують особливості будови кристалічної решітки, що пояснюють і проявляються властивості.
3. Сполуки вуглецю у вигляді кластерів. Така структура, при якій атоми утворюють особливу порожнисту зсередини конформацію, яку заповнюють водою або ядрами інших елементів. Приклади:
- вуглецеві наноконусы;
- астралены;
- диуглерод.

Фізичні властивості аморфного вуглецю
З-за великої різноманітності аллотропних модифікацій, виділити якісь загальні фізичні властивості вуглецю складно. Простіше говорити про конкретній формі. Так, наприклад, аморфний вуглець володіє наступними характеристиками.
- В основі всіх форм - дрібнокристалічні різновиди графіту.
- Висока теплоємність.
- Хороші провідникові властивості.
- Щільність вуглецю близько 2 г/см3.
- При нагріванні понад 1600 0відбувається перехід до графітові форми.
Сажа, деревне вугілля та кам'яні різновиди знаходять широке застосування в технічних цілях. Вони не є проявом модифікації вуглецю в чистому вигляді, проте містять його в дуже великій кількості.
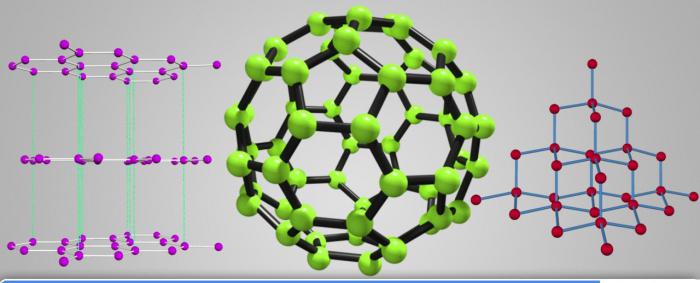
Кристалічний вуглець
Існує кілька варіантів, в яких вуглець - речовина, що формує правильні кристали різного виду, де атоми з'єднуються послідовно. У результаті відбувається утворення наступних модифікацій.
- Алмаз. Структура - кубічна, в якій з'єднуються чотири тетраедра. В результаті всі ковалентні хімічні зв'язки кожного атома максимально насичені і міцні. Це пояснює фізичні властивості: щільність вуглецю 3300 кг/м3. Висока твердість, низька теплоємність, відсутність електричної провідності - все це є результатом будови кристалічної решітки. Існують технічно отримані алмази. Утворюються при переході графіту в наступну модифікацію під впливом високої температури і певного тиску. У цілому температура плавлення алмазу так само висока, як і міцність - близько 3500 0С.
- Графіт. Атоми розташовані подібно структурі попереднього речовини, однак відбувається насичення лише трьох зв'язків, а четверта стає довшою і менш міцною, вона з'єднує між собою "шари" гексагональних кілець решітки. У результаті виходить, що графіт - м'яку, жирну на дотик речовину чорного кольору. Володіє хорошою електричною провідністю та має високу температуру плавлення - 3525 0С. Здатне до сублімації - сублімацію з твердого стану в газоподібний, оминаючи рідкий (при температурі 3700 0С). Щільність вуглецю - 2,26 г/см3, що набагато нижче такої у алмазу. Це пояснює їх різні властивості. З-за шаруватої структури кристалічної решітки, можливе використання графіту для виготовлення грифелів простих олівців. При проведенні по папері відшаровуються лусочки і залишають на папері слід чорного кольору.
- Фулерени. Відкриті були лише у 80-х роках минулого століття. Являють собою модифікації, в яких вуглеці з'єднуються між собою в особливу опуклу замкнуту структуру, що має в центрі порожнечу. Причому форма кристала - багатогранник, правильної організації. Кількість атомів парне. Найвідоміша форма фулерен60. Зразки подібного речовини були знайдені при дослідженнях:
- метеоритів;
- донних відкладень;
- фольгуритов;
- шунгитов;
- космічного простору, де містилися у вигляді газів.
Всі різновиди кристалічного вуглецю мають важливе практичне значення, оскільки володіють рядом корисних у техніці властивостей.
Хімічна активність
Молекулярний вуглець виявляє низьку хімічну активність внаслідок своєї стійкої конфігурації. Змусити його вступати в реакції можна лише повідомивши атому додаткову енергію і змусивши електрони зовнішнього рівня розпаритися. У цей момент валентність стає дорівнює 4. Тому у сполуках він має ступінь окислення + 2, + 4, - 4.
Практично всі реакції з простими речовинами, як металами, так і неметалами, протікають під впливом високих температур. Розглянутий елемент може бути як окислювачем, так і відновником. Однак останні властивості виражені у нього особливо сильно, саме на цьому грунтується застосування його у металургійній та інших галузях промисловості.
В цілому здатність вступати в хімічну взаємодію залежить від трьох факторів:
- дисперсності вуглецю;
- аллотропной модифікації;
- температури реакції.
Таким чином, у ряді випадків відбувається взаємодія з наступними речовинами:
- неметалами (воднем, киснем);
- металами (алюмінієм, залізом, кальцієм та іншими);
- оксидами металів та їх солями.
З кислотами та лугами не реагує з галогенами дуже рідко. Найважливіше з властивостей вуглецю - здатність утворювати довгі ланцюги між собою. Вони можуть замикатися в цикл, формувати розгалуження. Так відбувається утворення органічних сполук, які на сьогоднішній день обчислюються мільйонами. Основа цихсполук два елементи - вуглець, водень. Також до складу можуть входити і інші атоми: кисень, азот, сірка, галогени, фосфор, метали та інші.
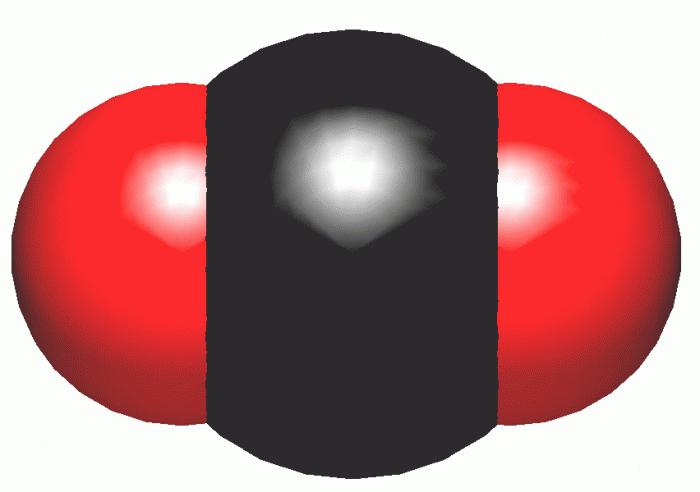
Основні сполуки та їх характеристика
Існує безліч різних сполук, до складу яких входить вуглець. Формула найвідомішого з них - 2 - вуглекислий газ. Однак крім цього оксиду, існує ще З - монооксид або чадний газ, а також недооксид32.
Серед солей, до складу яких входить цей елемент, найпоширенішими є карбонати кальцію і магнію. Так, карбонат кальцію має кілька синонімів у назві, так як в природі зустрічається у вигляді:
- крейди;
- мармуру;
- вапняку;
- доломіту.
Важливе значення карбонатів лужноземельних металів проявляється в тому, що вони активні учасники процесів утворення сталактитів і сталагмітів, а також підземних вод.
Вугільна кислота - ще одне поєднання, яке утворює вуглець. Формула її - Н23. Однак у звичайному вигляді вона вкрай нестійка і відразу ж у розчині розпадається на вуглекислий газ і воду. Тому відомі лише її солі, а не вона сама, як розчин.
Галогеніди вуглецю - виходять в основному непрямим шляхом, так як прямі синтези йдуть лише при дуже високих температурах і з низьким виходом продукту. Одне з найпоширеніших - CCL4 - тетрахлорметан. Отруйна з'єднання, здатне викликати отруєння при вдиханні. Отримують при реакціях радикального фотохімічного заміщення атомів водню в метані.
Карбіди металів - з'єднання вуглецю, в яких він проявляє ступінь окислення 4. Також можливе існування об'єднань з бором і кремнієм. Головна властивість карбідів деяких металів (алюмінію, вольфраму, титану, ніобію, танталу, гафнію) - це висока міцність і відмінна електропровідність. Карбід бору В4 - одне із самих твердих речовин після алмазу (9,5 по Моосу). Дані сполуки використовуються в техніці, а також хімічної промисловості, як джерела отримання вуглеводнів (карбід кальцію з водою призводить до утворення ацетилену і гідроксиду кальцію).
Багато сплави металів виготовляють з використанням вуглецю, значно підвищуючи тим самим їх якісні та технічні характеристики (сталь - сплав заліза з вуглецем).
Окремої уваги заслуговують численні органічні сполуки вуглецю, в яких він - основний елемент, здатний з'єднуватися з такими ж атомами в довгі ланцюги різної будови. До них можна віднести:
- алкани;
- алкени;
- арени;
- білки;
- вуглеводи;
- нуклеїнові кислоти;
- спирти;
- карбонові кислоти і багато інші класи речовин.
Застосування вуглецю
Значення сполук вуглецю і його аллотропних модифікацій в житті людини дуже велике. Можна назвати кілька найбільш глобальних галузей, щоб стало зрозуміло, що це дійсно так.
- Цей елемент утворює всі види органічного палива, з якого людина отримує енергію.
- Металургійна промисловість використовує вуглець як сильний відновник для добування металів з їх сполук. Тут же знаходять широке застосування карбонати.
- Будівництво та хімічна промисловість споживають величезна кількість сполук вуглецю для синтезу нових речовин і отримання необхідних продуктів.

Також можна назвати такі галузі господарства, як:
- ядерна промисловість;
- ювелірна справа;
- технічне обладнання (мастила, жароміцні тиглі, олівці та інше);
- визначення геологічного віку порід - радіоактивний індикатор 14;
- вуглець - чудовий адсорбент, що дозволяє використовувати його для виготовлення фільтрів.
Кругообіг в природі
Маса вуглецю, що знаходиться в природі, включена в постійний кругообіг, який циклічно відбувається щомиті по всій земній кулі. Так, атмосферне джерело вуглецю - СО2, поглинається рослинами і виділяється всіма живими істотами у процесі дихання. Потрапляючи в атмосферу, він знову поглинається, і так цикл не припиняється. При цьому відмирання органічних залишків призводить до вивільнення вуглецю і накопиченню його в землі, звідки потім він знову поглинається живими організмами і виводиться в атмосферу у вигляді газу.
Article in other languages:
AR: https://tostpost.com/ar/education/1741-carbon-is-carbon-atom-weight-of-carbon.html
BE: https://tostpost.com/be/adukacyya/3019-vuglyarod---geta-atam-vuglyarodu-masa-vuglyarodu.html
En: https://tostpost.com/education/18145-carbon-is-carbon-atom-weight-of-carbon.html
ES: https://tostpost.com/es/la-educaci-n/3022-el-carbono-es-el-tomo-de-carbono-masa-de-carbono.html
HI: https://tostpost.com/hi/education/1741-carbon-is-carbon-atom-weight-of-carbon.html
JA: https://tostpost.com/ja/education/1740-carbon-is-carbon-atom-weight-of-carbon.html
KK: https://tostpost.com/kk/b-l-m/3020-k-m-rtek---b-l-atom-k-m-rtek-bolady-massasy-k-m-rteg.html
PL: https://tostpost.com/pl/edukacja/3023-w-giel---to-atom-w-gla-masa-w-gla.html
PT: https://tostpost.com/pt/educa-o/3020-o-carbono-um-tomo-de-carbono-a-massa-de-carbono.html
TR: https://tostpost.com/tr/e-itim/3025-karbon---bu-karbon-atomu-a-rl-k-karbon.html

Alin Trodden - автор статті, редактор
"Привіт, Я Алін Тродден. Я пишу тексти, читаю книги і шукаю враження. І я непогано вмію розповідати вам про це. Я завжди радий брати участь у цікавих проектах."
Новини
Масштаби Всесвіту, будова, об'єкти
Були часи, коли світ людей обмежувався поверхнею Землі, що знаходиться у них під ногами. По мірі розвитку техніки людство розширив свій кругозір. Тепер люди замислюються про те, чи є межі у нашого світу і які масштаби Всесвіту? На...
Південний полюс і його підкорення. Яку географічну широту має Південний полюс?
На планеті є дві точки, які найбільш віддалені від лінії екватора. Це Північний полюс і Південний полюс. І якщо перший розташований посеред замерзлого океану, то другою знаходиться на тверді цього материка. Саме йому присвячена ця...
Кримська війна: коротко про причини і последсвиях
Кримська війна, коротко про яку мова піде нижче в статті, стала перехідним моментом для російських людей. Це пов'язано, насамперед, з її результатами. Народ і влада усвідомлюють необхідність перетворень у країні. Сумні підсумки ск...
Прийменники похідні й непохідні: правило, список, приклади
Похідний і непроизводный привід, в першу чергу, є службовою частиною мови. Він пов'язує слова між собою і показує їх залежність один від одного. Окремо використовуватися прийменники не можуть, вони завжди стоять біля займенників, ...
Хто такий Ломоносов Михайло Васильович: біографія і творчість
Лише невгамовна пристрасть до знань допомогла синові селянина стати основоположником таких напрямів науки, як природознавство, хімія, астрономія, приладобудування, географія, металургія, геологія, філологія. Ломоносов - один з най...
Відродження: що таке Ренесанс і які його наслідки?
Історія знає кілька поворотних подій і явищ, які повністю міняли картину світу її жителів. Одним з таких рубежів стало Відродження. Що таке Ренесанс (ці терміни рівнозначні)?Основні риси РенесансуВідродженням називають епоху, яка ...






















Примітка (0)
Ця стаття не має коментарів, будьте першим!