Agregada do estado de sal. O sal comum, química
Mais de 10 milhões de compostos orgânicos e mais de 500 mil inorgânicos, conhecido químico qualificados hoje em dia. Entre eles, há um sofisticado para a estrutura e as propriedades que se aplicam apenas a produtos químicos ou para fins médicos. E há aqueles, que não é difícil organizados e são muito comuns em residências. Mas não menos importantes e significativos. Numa dessas substâncias se refere o sal comum. Em casa chamam-lhe a mais de alimentos e na indústria química chamam de cloreto de sódio ou cobalt sódio. Em uma indústria é chamada de um mineral, o que ela faz na natureza, галитом, bem como de sal grosso ou sólido sal grosso. Considere mais agregada do estado de sal, a estrutura, as propriedades, o espólio, a aplicação e a história da introdução em massa para o consumo.

Em quais estados há sal?
O Que é uma condição de substâncias e como é que acontece? Isso depende de qual substância em questão. Cada aprendiz com idade inferior a 7 classe pode ser chamado agregada do estado de sal, porque é a substância que está em cada casa. Hoje, sem ele, é difícil para o homem moderno imaginar a sua vida. Além disso agregada do estado de sal é evidente a olho nu - os finamente ou grosseiramente dispersar o coliseu do céu correta forma cúbica. No entanto, растворив sal na água, nós receberemos um agregado o estado líquido. O mesmo receberemos se apenas расплавим cristais em alta temperatura. A única condição que, para o sal não é típico, é o gasoso. Mas, sob certas condições, pode receber e-lo.
Mais:
A história do desenvolvimento da tecnologia de computação
Os primeiros dispositivos de computação foram os próprios dedos de uma pessoa. Quando a ferramenta foi suficiente, no curso de iam pedras, galhos, conchas. Dobrando-se de um conjunto de dezenas, depois centenas, o homem aprendeu a contar e usar as fe...
O impulso nervoso, a sua conversão e o mecanismo de transmissão
O sistema Nervoso humano atua como uma espécie de coordenador no nosso corpo. Ela passa o comando do cérebro musculatura, órgãos, tecidos e processa os sinais de longo alcance deles. Como uma espécie de suporte de dados, é usado o impulso nervoso. O ...
Canal do panamá: um ano, a abertura oficial do objecto e a sua importância histórica
Durante séculos, a humanidade tenta recriar condições naturais da Terra, com o objetivo de receber quaisquer benefícios. Um desses casos, a adaptação é do canal do Panamá, o ano, a abertura oficial deste objeto foi marcado por um evento, повлиявшим p...
Condições para a mudança agregada de estado
- Para obter o sal no estado líquido, através da fusão de cristais sólidos de origem natural, tem de aplicar-se a temperatura, igual a 800OС.
- Para a tradução de sal no estado gasoso расплавленные cristais precisa ferver (cerca de 1400O) e deixe ferver, até a completa transição componentes estruturais em íons (Na+ CLO).
- Firme agregada do estado de sal de cozinha é a sua aparência natural em condições naturais.

Por que ocorre essa variação de temperatura lidando com cristais? Isto é devido a estrutura cristalina da rede.
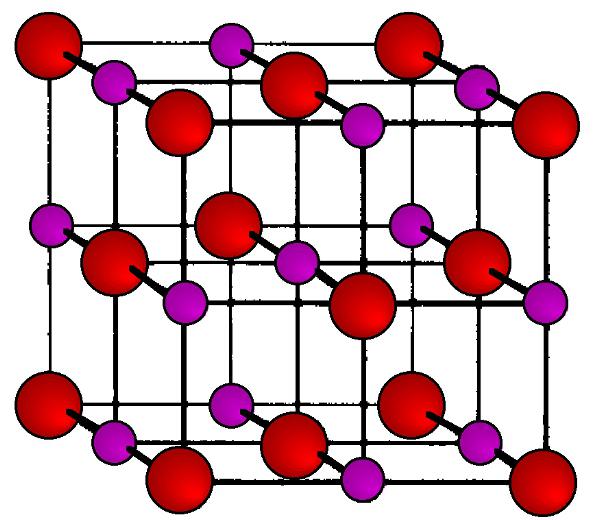
Grade Cristalina
Ele é um corretas гранецентрированные cúbicos cristais transparentes. Em cada canto do cubo (nós da grade cristalina) estão distribuídos íons carregados positivamente Na+ e íons carregados negativamente CLO. Graças drasticamente различающейся электроотрицательности desses átomos entre eles ocorre tão forte atração eletrostática, o que para a destruição deve ser aplicado a condições severas (altas temperaturas, impacto mecânico). Este tipo de cristal da grade leva o nome de ião, e é característico para todos os sais alcalinos, germacreno e metais de transição.
É por isso que a temperatura de sal (como o ponto de fusão e de ebulição) é tão alto. No entanto, você pode obter os cristais não apenas de forma cúbica, mas em forma de pirâmide (de oito, doze e двадцатигранной). Para isso, basta regular a temperatura de evaporação do chorume de uma determinada maneira. Em qualquer caso, a cavidade interna dos cristais permanece cheia de líquido, quando se trata de uma solução de sal em água.
Fórmula Química cloreto de sódio é simples e é expressa элементным composição de NaCL.
Propriedades Físicas галита
Propriedades Físicas do cloreto de sódio, é possível descrever vários itens:
- Solid cristais de branco, de rosa, de azul, e de púrpura, da cor vermelha. A coloração depende da existência de impurezas na extração. Pura substância cristalina, de cor branca.
- Se Dissolve em água, na proporção de cerca de 100/30 (em 100 g de água 30 g de sal). Boa solubilidade explica a presença dos dipolos da água, que se associam em torno de si os íons de sódio e de cloro, causando a destruição da eletrostática de atração entre eles e, como conseqüência, a destruição da grade cristalina.
- Derretido e ferve a temperaturas elevadas (800-1400O).
- Tem mal уловимый um cheiro agradável.
- Sal a gosto.

Propriedades Químicas de cloreto de sódio
Como qualquer dissolvida a média de sal, cloreto de sódio é capaz de entrar em interação com o:
- Outros sais de acordo com a reação de troca (pré-requisito: a reação de alocação de gás, a precipitação ou a educação малодиссоциируемого da substância): NaCL + AgNO3 = NaNO3 + AgCL (branco творожистый sedimentos). É uma qualidade reação do íon CL.
- Com os metais, que se encontra na ЭХРНМ à esquerda de sódio: A + NaCL = KCL + Na.
- Dissociado em solução aquosa disponíveis гидратированные диполями de água de jonas: NaCL (water p-p) = Nd+ + CLO. O resultado é uma solução de sal de cozinha, que é um eletrólito forte.
- Hidrólise não está exposto, assim como é sal, formado por um ácido forte e uma base forte.
- Com a electrólise (ação de uma corrente elétrica) decompõe-se com a formação de produtos livres ede hidróxido de sódio (cáustica): NaCL = Na + Cl2 + NaOH.
, Onde a natureza contém cloreto de sódio?
Atualmente, o sal comum - a substância, freqüentemente encontrados na natureza. E embora sempre foi assim, mas nos tempos antigos e tempos da idade média, ele era considerado um produto muito caro. Tudo isso porque não sabia de métodos de extração de sal a partir de fontes naturais. E tais fontes mundiais de estoques muito - галит é considerada quase ilimitado de recurso natural. Onde está o sal está na natureza?
- Os Mares e oceanos de água salgada.
- Lagos Salgados.
- Salgados fontes.
- água Subterrânea.
- Água de estuários.

A Extração de галита
A Extração e refino de sal têm a sua tecnologia, simplesmente porque extraído de uma substância mais frequentemente do que para o consumo inútil devido ao elevado teor de impurezas. Extraído галит de diferentes maneiras, por exemplo:
- Através de obras subterrâneas;
- Dos reservatórios no fundo de uma mina de sal de corpos de água;
- выпариванием ou вымораживаем de água salgada e de água do mar ou de água do oceano;
- выпариванием de águas subterrâneas.
De Qualquer maneira dá a oportunidade de obter cristais галита. No entanto, para consumo humano, eles devem passar a outro tipo de tratamento - moagem. Afinal, dificilmente alguém usa em casa quando estiver a cozinhar um grande cristal de sal. Mais frequentemente do que o seu adquirem já sem impurezas, измельченном quase em pó. Também existem tipos de sal iodado, fluorada e assim por diante não só para alimentar, mas também para fins técnicos.
Aplicação de pedra de sal
A aplicação e o uso de cloreto de sódio são bastante extensas. Os principais deles, juntamente com exemplos e os resultados são mostrados na tabela.
| O Setor | A Base o uso de sal | Resultado |
| Paisagem construção | A flexibilização do solo em baixas temperaturas e eliminação de fugas de água | Construção de canais de irrigação e reservatórios de água |
| Medicina | Semelhança da solução de sal com o sangue de uma pessoa. Кровезаменяющий solução de cloreto de sódio a 0,85%), chamado de soro fisiológico | Restauração arterial equilíbrio após uma extensa кровепотерь, normalização do trabalho натрие-potássio bomba no sistema cardiovascular, a manutenção da constância da composição do suco gástrico |
| Química | Sínteses praticamente significativas de substâncias a base de matérias-primas de cloreto de sódio | São: bicarbonato de sódio, ácido clorídrico, metal sódio, cloro, hidróxido de sódio, de vidro, de plástico, de sabonete, papel e outros produtos |
| Alimentos | Anti-séptico e antibacteriano ação de sal | Conservas de alimentos (carne, peixe, legumes), a melhoria do gosto qualidades de alimentos |
| Metalúrgica | Propriedades Físicas e químicas de sal | Obtenção de alumínio, солевых pilhas, filtros |
| Кожевенная | Anti-séptico e antibacteriano ação de sal | Processamento de peles e couro cru indústria de curtumes |
História do surgimento em casa
O Sol apareceu nas mesas em cada casa, de longe, não imediatamente. Uma vez que ela era vale seu peso em ouro, e em um sentido muito real. Ainda no século XVIII, alguns povos da África trocaram a um punhado de sal grosso um punhado de areia dourada. Um pouco mais tarde, na Etiópia, pedaços os de sal foram a moeda padrão. Na Roma Antiga militares легионерам mesmo mensal, o salário mascarou essa substância, o que eventualmente levou à называнию seus soldados. As crianças pobres dos povos africanos apenas lambeu, de pedra, pedaços de повареной sal como guloseima. Na Holanda, ela é usada para punir os criminosos, para a tortura. Quilty, geralmente, não deram o sal, e o homem em pouco tempo morreu.
A Primeira vez que seleccionar e consumir alimentos é uma substância as pessoas aprenderam ainda na antiguidade. Então, foi descoberto que o sal está contido em plantas. Portanto, a sua queimados e as cinzas usado como tempero. Mais tarde, na China, aprendeu a выпаривать o sal da água do mar, e o processo de desenvolvimento de métodos para sua obtenção começou a avançar mais rápido.

Na Rússia, o sal extraído dos lagos (os mais famosos lagos da Rússia até agora - Эльтон e Baskunchak). Então промысловое o valor de uma substância era um fenômeno muito raro. Encontram-lo apenas alguns mercadores, que, em seguida, vendidos a preços exorbitantes. Dar ao luxo de ter o sal poderia só os ricos e famosos de pessoas. Com o tempo a produção e a extração de наладились. Começou a ser utilizada de diferentes formas de extração e processamento, e hoje em dia uma das mais comuns domésticos substâncias - sal. A química deste composto, propriedades, aplicações na medicina e em outros setores tornaram-se conhecidos, aproximadamente, do século XVI-XVII séculos.
Um Estudo no distrito escolar de curso
O Estudo da estrutura e do agregado do estado, bem como das propriedades químicas do sal começa com a escola, dentro de tal disciplina, como a química (classe 8). Sal no distrito escolar de curso a ser exploradas em toda a sua diversidade na natureza. Os alunos recebem noções sobre química de base empírica, fórmulas, propriedades físicas e químicas. Para a facilidade e comodidade de memorização de fórmulas e propriedades físicas na dedicatória do tutorial, normalmente, encontram-sal, a tabela, que dá uma idéia sobre a sua solubilidade em água. Lá você pode encontrar informações sobre a solubilidade de ácidos, bases e fundamentos.

Uma característica Importante de sais é a sua плавкость, na base sobre a qual também é construída a sua extração na natureza. Os alunos a navegar facilmente em desafios плавкость de sal. A tabela e os gráficos permitem não só de ver, легкоплавко substância ou тугоплавко, mas também para determinar o exemplar do ponto de fusão e ponto de ebulição. Geralmente, essas tabelas encontram-se em livros didáticos ("Química", de 8 de classe). O sal deve ser aprendida no contexto de tais ciências, como a biologia e a física. Portanto, um conjunto de tarefas para os alunos é construído exatamente sobre a integração межпредметных links.
Article in other languages:
AR: https://tostpost.com/ar/education/7206-the-aggregate-state-of-the-salt-salt-chemicals.html
BE: https://tostpost.com/be/adukacyya/12890-agregatny-stan-pavaranay-sol-pavaranaya-sol-h-m-ya.html
DE: https://tostpost.com/de/bildung/12892-aggregatzustand-des-kochsalzes-kochsalz-chemie.html
En: https://tostpost.com/education/20635-the-aggregate-state-of-the-salt-salt-chemicals.html
ES: https://tostpost.com/es/la-educaci-n/12900-un-estado-de-la-sal-la-sal-com-n-la-qu-mica.html
HI: https://tostpost.com/hi/education/7208-the-aggregate-state-of-the-salt-salt-chemicals.html
JA: https://tostpost.com/ja/education/7207-the-aggregate-state-of-the-salt-salt-chemicals.html
KK: https://tostpost.com/kk/b-l-m/12894-agregatty-zhay-k-y-as-t-zy-as-t-zy-himiya.html
PL: https://tostpost.com/pl/edukacja/12890-stanu-skupienia-soli-s-l-chemia.html
TR: https://tostpost.com/tr/e-itim/12895-fiziksel-durum-tuz-tuz-kimya.html
UK: https://tostpost.com/uk/osv-ta/12892-agregatniy-stan-kuhonno-sol-kuhonna-s-l-h-m-ya.html
ZH: https://tostpost.com/zh/education/7838-the-aggregate-state-of-the-salt-salt-chemicals.html

Alin Trodden - autor do artigo, editor
"Olá, sou o Alin Trodden. Escrevo textos, leio livros e procuro impressões. E eu não sou ruim em falar sobre isso. Estou sempre feliz em participar de projetos interessantes."
Notícias Relacionadas
Russo estado hidrometeorológica universidade: endereço, faculdades
Na Rússia, muitos exclusivos de instituições de ensino superior, mas o mais especial é hidrometeorológica universidade, um em São Petersburgo. Tal faculdade apenas um em nosso país. A singularidade de organização educacional, ofer...
Престидижитатор - o que é? A origem e o uso da palavra
No popular soviética conto "Bárbara de beleza - longa trança" é mencionada a palavra interessante "престидижитатор". E, apesar de lá mesmo, uma explicação "ихнему, é престидижитация, e o nosso agilidade dos pés e hipnose", nem sem...
Oblast de conservatório - alma mater, em estilo gótico
o cartão de Visita da cidade de Saratov, por direito, é a Saratov conservatório nome Л. Собинова. Excepcionalmente, a arquitetura gótica, que não se repete em nenhum outro lugar nos edifícios da cidade, se destaca por sua sofistic...
O entusiasmo é... o Significado da palavra entusiasmo, sinônimos e antônimos
Muito agradável sensação é a emoção. Isto é, quando sente o aumento do desejo de fazer alguma coisa. A maioria dos воодушевляются perspectivas e o movimento para a frente. Para alguns, particularmente bom humor causam uma variedad...
Nicholas Власик: biografia e vida pessoal do chefe de protecção de Stalin
Em junho de 2000, a decisão do Supremo tribunal da Rússia foi postumamente exonerado ex-chefe da guarda pessoal de Stalin, o tenente-general Nikolai Власик cuja biografia se tornou a espinha dorsal deste artigo. Como foi no banco ...
A estrutura de um neurônio e sua função морфофизиологические
um Neurônio, sendo estrutural e funcional unidade básica do sistema nervoso é uma высокоспециализированную célula, que é capaz de gerar e conduzir impulsos elétricos. Durante o processo de evolução neurônios perderam a capacidade ...





















Comentários (0)
Este artigo possui nenhum comentário, seja o primeiro!