Propiedades químicas de glicol de etileno, la característica. Двухатомный alcohol. Éteres de glicol de etileno
Las Más conocidas y usadas en la vida de la persona y en la industria de la sustancia, pertenecen a la categoría de многоатомных alcoholes – es el glicol de etileno y la glicerina. El estudio y el uso comenzó hace varios siglos, pero las propiedades de estos compuestos orgánicos en gran medida son diferentes y únicos, lo que los hace indispensables hoy en día. Многоатомные los alcoholes se utilizan muchos químicos синтезах, sectores y áreas de la actividad vital humana.
La Primera introducción» con etilenglicol y la glicerina: la historia de la recepción de
En 1859, a través de la двухстадийного de un proceso de interacción дибромэтана con ацетатом de la plata y el posterior procesamiento de acre cali obtenido en la primera reacción этиленгликольдиацетата, charles Вюрц sintetizó por primera vez el glicol de etileno. Algún tiempo más tarde, se desarrolló un método directo de la hidrólisis de la дибромэтана, pero a escala industrial a principios del siglo xx двухатомный alcohol 1,2-диоксиэтан, él mismo – monoetilenglicol, o simplemente glicol, en los estados unidos recibieron a través de la hidrólisis de la этиленхлоргидрина.
Hoy En día en la industria y en el laboratorio aplican una serie de otros métodos nuevos, más eficientes, con materias primas y de energía de puntos de vista, y ecológicos, así como la aplicación de los reactivos que contienen o emiten el cloro, las toxinas, carcinógenos y otras sustancias peligrosas para las personas y el medio ambiente de la sustancia que se reduce a medida que el desarrollo de la verde» la química.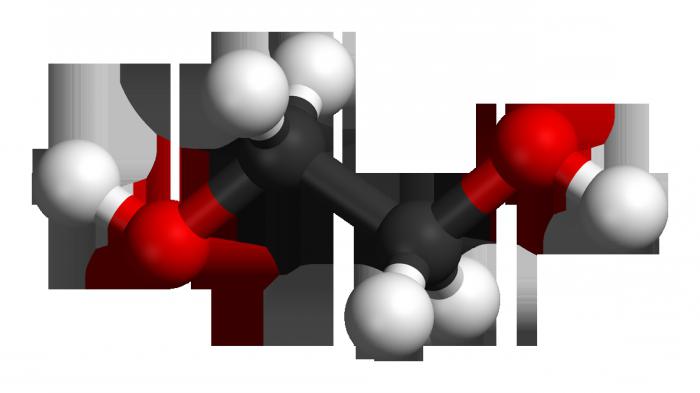
El Boticario, carlos por wilhelm scheele en 1779, se abrió la glicerina y características de la composición de la conexión estudiado en 1836 Теофиль, jules Пелуз. Dos décadas más tarde, se instaló y justificación de la estructura de las moléculas de este трехатомного de alcohol en los escritos de pierre eugène Марселея Вертело y charles Вюрца. Por último, veinte años después, charles friedel realizó la síntesis completa de la glicerina. En la actualidad, la industria utiliza dos métodos para su obtención: a través de cloruro de alilo de polipropileno, así como a través de la acroleína. Propiedades químicas этиленгиликоля, como la glicerina, usan ampliamente en las diferentes esferas de la producción química.
Más:
El general walter von Reichenau: su biografía, sus logros y la historia
El General mariscal de campo de la alemania nazi walter von Reichenau (Walter von Reichenau) se contaba entre los pocos altos oficiales del ejército de la wehrmacht, que apoyó activamente el nazismo. Durante la Segunda guerra mundial fue comandante d...
Trajes espaciales de los astronautas: de la asignación de la unidad. El primer traje espacial
Trajes espaciales de los astronautas – no es simplemente trajes de vuelo en órbita. El primero de ellos se remonta a principios del siglo veinte. Era la época de antes de los vuelos espaciales restaba casi medio siglo. Sin embargo, los científi...
Oriental de la plataforma europea: forma de alivio. Minerales oriental de la plataforma europea
La Mayor parte del territorio europeo de rusia, así como de algunos países de la cei se encuentra en la parte continental de un tramo de la corteza terrestre, que lleva el nombre oriental de la plataforma europea. La forma del relieve aquí es predomi...
La Estructura y la estructura de la conexión
En la base de la molécula est непредельный hidrocarburo esqueleto de etileno, que consta de dos átomos de carbono, en el que se produjo una ruptura de un enlace doble. En vacantes валентные el lugar de los átomos de carbono se unieron los dos grupos hidroxi. La fórmula de etileno –2H4, después de la ruptura de кранной de la comunicación y de la adhesión de гидроксильных grupos (a través de varias etapas) se ve como Con2H4(ÉL)2. Este es el glicol de etileno.
La Molécula de etileno es inherente a la estructura, mientras que двухатомный el alcohol tiene una especie de trans-конфигурции en la colocación de la гидроксильных grupos con respecto al carbono остову y el uno al otro (plenamente este término se aplica a la posición respecto a un múltiplo de la comunicación). Tal despliegue responde a una ubicación remota водородов de grupos funcionales, de menor energía, y significa – la máxima estabilidad del sistema. En pocas palabras, una SE-grupo mira» hacia arriba y la otra hacia abajo. Al mismo tiempo volátiles son compuestos con dos гидроксилами: cuando un átomo de carbono, образуясь en la mezcla de reacción, inmediatamente дегидратируются, pasando en aldehídos.
Clasificación de la pertenencia
Propiedades Químicas de glicol de etileno se definen sus orígenes, de un grupo de многоатомных alcoholes, a saber, el subgrupo диолов, es decir, compuestos con dos гидроксильными segmentos adyacentes de átomos de carbono. La sustancia, también contienen varios ESTÁ de suplente, es y glicerina. Tiene tres paños de limpieza con alcohol funcionales del grupo y es el más común, como representante de su división.
Muchos de los compuestos de esta clase también se adquieren y utilizan en la fabricación de sustancias químicas para diferentes синтезов y otros objetivos, pero el uso de glicol de etileno tiene más graves y hay en casi todos los sectores de la industria. Este tema se analizará en detalle más adelante.
Características Físicas
El Uso de glicol de etileno se explica por la presencia de una serie de propiedades que le son inherentes многоатомным спиртам. Es una de las características distintivas específicas para esta clase de compuestos orgánicos.
Lo Más importante de las propiedades de la – es ilimitada la capacidad de mezclarse con N2Oi Agua + etilenglicol da la solución, con una única característica: la temperatura de su punto de congelación en función de la concentración de diola, por debajo de 70 grados, lo que el puro destilado. Es importante señalar que esta dependencia no lineal, y por la consecución de un determinado contenido cuantitativo de glicol comienza el efecto contrario – la temperatura de congelación aumenta con el porcentaje de растворяемого de la sustancia. Esta característica se encontró la aplicación en el ámbito de la producción de varios de los anticongelantes, líquidos незамерзаек», que se cristalizan extremadamente bajas térmicas, de las características del medio ambiente.
Además, como en el agua, el proceso de disolución de la perfección pasa en alcohol y acetona, pero no se observa en парафинах, бензолах, ésteres y тетрахлорметане. A diferencia de su алифатического el fundador de este gaseoso de una sustancia, el etileno, glicol – es сиропоподобная,transparente, con un pequeño matiz amarilloel líquido, сладковатая al gusto, con atpico olor, casi нелетучая. La congelación completo de glicol de etileno se produce cuando - 12,6 grados celsius, y la ebullición – a +197,8. En condiciones normales la densidad es de 1,11 g/cm3.
Métodos
El Etilenglicol puede obtener de varias maneras, algunos de ellos hoy tienen sólo histórico o препаративное valor, mientras que otros se utilizan activamente el hombre en cantidades industriales y no sólo. Siguiendo un orden cronológico, considere más importantes.
Por Encima de las ya fue descrito por el primer método para la obtención de glicol de etileno de дибромэтана. La fórmula de etileno, doble cuya relación está rota, y libres de valencia ocupados halógenos, el principal de la sustancia original en esta reacción, además de carbono e hidrógeno se compone de dos átomos de bromo. La educación intermedia de conexión en la primera etapa del proceso, es posible justamente gracias a su отщеплению, es decir, la sustitución ацетатными grupos, que si el futuro de hidrólisis, se convierten en alcohol.
El desarrollo de la ciencia ha sido posible obtener el glicol de etileno directa гидролизом cualquier этанов sustituido dos halógenos adyacentes de átomos de carbono, con la ayuda de soluciones acuosas de los carbonatos de los metales alcalinos grupo o (menos respetuoso con el medio ambiente reactivo) N2Y dióxido de plomo. La reacción es bastante laborioso» y se realiza sólo cuando es significativamente elevadas temperaturas y presiones, pero esto no impidió que los alemanes en los períodos de las guerras mundiales, el uso de este método para la producción de etilenglicol en escala industrial.
Su papel en el proceso de formación de la química orgánica ha jugado y la forma de obtener el glicol de etileno de этиленхлоргидрина mediante su hidrólisis con sales de metales alcalinos grupo. Al aumentar la temperatura de reacción hasta 170 grados de salida de destino del producto ha alcanzado el 90 %. Pero fue una considerable falta de – glicol para extraer, a partir de la solución de sal, lo que directamente implica una serie de retos. Los científicos han decidido esta cuestión, estableciendo un método con el mismo origen de la sustancia, pero dividiendo el proceso en dos etapas.
La Hidrólisis этиленгликольацетатов, como anteriormente final de etapa método de Вюрца, se convirtió en independiente de la forma, cuando fueron capaces de obtener el reactivo de oxidación de etileno en ácido acético oxígeno, es decir, sin el uso de costosos y muy неэкологичных compuestos halógenos.
También se Sabe que muchos de los métodos de producción de glicol de etileno a través de la oxidación de etileno гидроперекисями, перекисями, orgánicos надкислотами en presencia de catalizadores (conexiones осмия), хлоратом de potasio y otros, También existen electroquímicas y la radiación métodos químicos.
Característica general de las propiedades químicas
Propiedades Químicas de glicol de etileno se definen en sus grupos funcionales. En las reacciones puede participar una гидроксильный el vicepresidente o ambos, dependiendo de las condiciones de proceso. La principal diferencia en la reactividad es que, a través de la presencia de многоатомного alcohol pocos гидроксилов y su influencia mutua se manifiestan más fuertes ácidos propiedades que одноатомных "hermanos". Por lo tanto, en las reacciones con los álcalis productos son de sal (para el glicol – гликоляты, para la glicerina – глицераты).
En las propiedades químicas del glicol de etileno, así como la glicerina, incluye todas las reacciones de alcoholes de la categoría de одноатомных. Glicol da completos e incompletos ésteres en las reacciones con одноосновными ácidos, гликоляты, respectivamente, se forman con metales alcalinos, y al proceso químico con ácidos fuertes o sus sales se destaca aldehído acético mediante la отщепления de la molécula, el átomo de hidrógeno.
La Reacción de activos de metales pesados
La Interacción de glicol de etileno, con activos de metales (de pie después del hidrógeno en la serie de tensiones) a temperaturas elevadas da этиленгликолят correspondiente de metal, más se libera hidrógeno.
2H4(ÉL)2 + X →2H4O2X, donde X – el activo двухвалентный metal.
Cualitativa de la reacción en el etilenglicol
Distinguir многоатомный alcohol de cualquier otro líquido que se puede con la ayuda visual de la reacción característica sólo para esta clase de compuestos. Para ello, a бесцветному solución de alcohol vierten свежеосажденный hidróxido de cobre (2), que tiene la característica tonalidad azul. Al interactuar mixtas de los componentes se produce la disolución del calado y la coloración de la solución en el lleno de color azul - como resultado de la educación гликолята de cobre (2).
Polimerización
Propiedades Químicas de glicol de etileno, son de gran importancia para la producción de solventes. Межмолекулярная la deshidratación de la mencionada sustancia, es decir, desmenuzar el agua de cada una de las dos moléculas de glicol y su posterior fusión (un grupo hidroxilo отщепляется totalmente, y de la otra que sale sólo de hidrógeno), da la posibilidad de obtener un disolvente orgánico – диоксана, que a menudo se utiliza en química orgánica, a pesar de su elevada toxicidad.
Cambio de hidroxilo en halo
En La interacción de glicol de etileno con галогеноводородными ácidos se observa la sustitución de гидроксильных grupos pertinentes de halógenos. El grado de sustitución depende de la мольной de la concentración de галогенводорода enla mezcla de reacción:
PERO-ch2-ch2-L + 2НХ → X-ch2-ch2-X, donde X – el cloro o el bromo.
La Obtención de ésteres
En las reacciones de glicol de etileno con ácido nítrico (de una concentración determinada) y одноосновными ácidos orgánicos (fórmico, acético, propiónico, aceitosa, валерьяновой, etc.) se produce la formación de complejos y, en consecuencia, simples моноэфиров. En otros, la concentración de ácido nítrico – di - y тринитроэфиров de glicol. Como catalizador se utiliza el ácido sulfúrico determinada concentración.
Esenciales derivados de glicol de etileno
Valiosas sustancias que se pueden obtener de многоатомных alcoholes sencillos de las reacciones químicas (descritos anteriormente), son ésteres de glicol de etileno. A saber: монометиловый y моноэтиловый, la fórmula que - NO-ch2-ch2-De-ch3 y NO-ch2-ch2-2H5, respectivamente. De las propiedades químicas son similares en muchos aspectos a los glicoles, pero, así como de cualquier otra clase de compuestos, tienen una reacción las características inherentes sólo a ellos:
- Монометилэтиленгликоль es un líquido sin color, pero con la característica отвратным olor, закипающую cuando 124,6 grados centígrados, bien растворяющуюся en etanol, otros disolventes orgánicos y agua, mucho más летучую de glicol, y con una densidad menor, que el agua (del orden de 0,965 g/cm3).
- Диметилэтиленгликоль – también el líquido, pero con menos olor característico, con una densidad de 0,935 g/cm3, la temperatura de ebullición de 134 grados por encima de cero y la solubilidad de la comparativa con el anterior gomologom.
El Uso de целлозольвов en los que genéricamente se conoce como моноэфиры el glicol de etileno es bastante común. Se utilizan como reactivos y disolventes en síntesis orgánica. También se aplican y sus propiedades físicas escudo anti-corrosión y антикристаллизационных aditivos anticongelantes y aceite de motor.
El uso y la política de precios producido una serie de
El Costo de las fábricas y empresas dedicadas a la fabricación y venta de estos productos químicos, que oscila en un promedio de alrededor de 100 rublos por kilogramo de este compuesto químico, como el etilenglicol. El precio depende de la pureza de la sustancia y el máximo de porcentaje de destino del producto.
El Uso de glicol de etileno no se limita a una sola área. Así, como materia prima que se utiliza en la fabricación de disolventes orgánicos, resinas artificiales y fibras, líquidos, замерзающих a bajas temperaturas. Él está involucrado en muchos sectores industriales, tales como la automotriz, aeronáutica, farmacéutica, eléctricos, cuero, tabaco. Hecho significativo de su valor para la síntesis orgánica.
Es Importante recordar que el glicol – es tóxica conexión, que puede causar un daño irreparable a la salud humana. Por lo tanto, su almacenan en recipientes herméticos de aluminio o de acero obligatorio interior de una capa que protege el tanque contra la corrosión, sólo en posiciones verticales y zonas que no estén provistos de fuentes de calor de los sistemas, pero con buena ventilación. El plazo de – no más de cinco años.
Article in other languages:

Alin Trodden - autor del artículo, editor
"Hola, soy Alin Trodden. Escribo textos, leo libros y busco impresiones. Y no soy mala para decírtelo. Siempre estoy feliz de participar en proyectos interesantes."
Noticias Relacionadas Con La
las Semejanzas y diferencias entre la persona y el animal es muy interesante el tema. Después de Horas de darwin creó su evolutiva de la teoría, comenzaron las interminables disputas sobre si realmente los humanos evolucionamos de...
Cómo era alejandro 2? La personalidad del emperador. Biografía, los años de gobierno de
el Primer día de primavera de 1881, fue обагрен sangre del emperador, ha iniciado en la historia de rusia como un gran explorador de la reforma, sobre el derecho de заслужившего dada a él por el pueblo epíteto de el libertador. En...
Característica de los héroes. "Granate pulsera de Куприна
el Héroe de la historia Granate pulsera» ¡ una de las más conmovedoras imágenes en la literatura. Sobre el manuscrito de esta obra, lloró el propio autor. Kuprin afirmaba que él es el más casto de todo lo que él ...
¿Qué es la materia oscura? Si existe la materia oscura?
la Cuestión del origen del Universo, de su pasado y el futuro le importa un comino la gente desde tiempos inmemoriales. A lo largo de muchos siglos, la teoría de la surgían y se niega, ofreciendo una visión del mundo basada en dat...
Los láseres de estado sólido: tipos, la unidad, el principio de trabajo, la aplicación de
Los láseres de estado sólido son cuánticos de los generadores a base de semiconductores medio activo, en el que la óptica de la ganancia se genera a la radiación cuando квантовом la transición entre niveles de energía con una gran...
cómo se relacionan las actividades y las necesidades, se dice mucho. Hay enteras de científicos, dedicados a este tema. Realmente es muy interesante y diversa. Toda su debatir difícil, ya que la esencia se refiere a el desconocido...






















Comentarios (0)
Este artículo no tiene comentarios, se el primero!