Now - 21:16:19
Формула кисню. Періодична таблиця Менделєєва - кисень
Хімічний елемент кисень знаходиться у другому періоді VI-ої головної групи застарілого короткого варіанту періодичної таблиці. За новими стандартами нумерації — це 16-я група. Відповідне рішення прийнято ІЮПАК в 1988 році. Формула кисню як простої речовини 2. Розглянемо його основні властивості, роль у природі та господарстві. Почнемо з характеристики всієї групи періодичної системи, яку очолює кисень. Елемент відрізняється від споріднених йому халькогенов, а вода відрізняється від водневих сполук сірки, селену і телуру. Пояснення всім відмінних рис можна знайти, тільки дізнавшись про будову і властивості атома.
Халькогены — родинні кисню елементи
Подібні за властивостями атоми утворюють одну групу в періодичній системі. Кисень очолює сімейство халькогенов, але відрізняється від них по ряду властивостей.
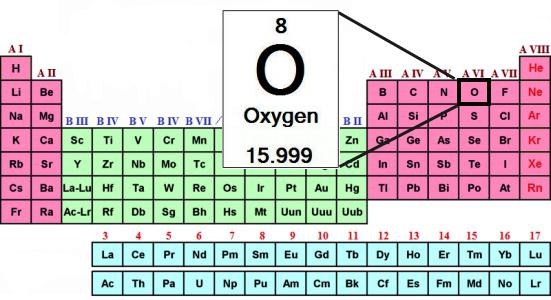
Атомна маса кисню — родоначальника групи — складає 16 а. е. м. Халькогены при утворенні сполук з воднем і металами проявляють свою звичайну ступінь окислення: –2. Наприклад, в складі води (Н2) окислювальне число кисню одно –2.
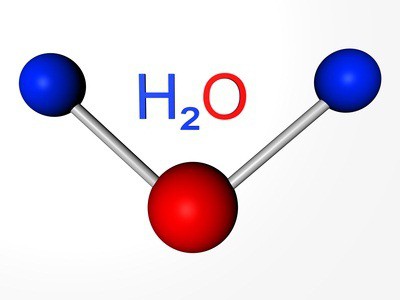
Склад типових водневих сполук халькогенов відповідає загальній формулі: Н2R. При розчиненні цих речовин утворюються кислоти. Тільки водневе з'єднання кисню — вода — володіє особливими властивостями. Згідно з висновками вчених, це незвичайне речовина є дуже слабкою кислотою, і дуже слабким підставою.
Сірка, селен і телур мають типові позитивні ступені окиснення (+4, +6) у сполуках з киснем та іншими неметалами, що володіють високою электроотрицательностью (ЕО). Склад оксидів халькогенов відображають загальні формули: RO2, RO3. Відповідні їм кислоти мають склад: H2RO3, H2RO4.
Більше:
Перший штучний супутник Землі є одним з найбільших досягнень науки ХХ століття. Тим не менш, як це ні парадоксально, цьому великому науковому і технічному досягненню значною мірою сприяла холодна війна між двома наддержавами: США і Радянським Союзом....
Що таке соціалізація, і як вона змінює людину
Спробуємо розібратися, що таке соціалізація, в чому її сутність і особливість. Адже для кожної особистості входження у суспільство і засвоєння його основних норм є фундаментом до подальшої безпроблемною і успішного життя і діяльності. Отже, що таке с...
Принц Чарльз – головний спадкоємець британського престолу
Згідно із законом королівства Великобританія, спадкоємець британського престолу - це старший закононароджена син чинного монарха або ж попереднього претендента на престол. Однак якщо у царюючого особи немає дитини чоловічої статі, то право спадкуванн...
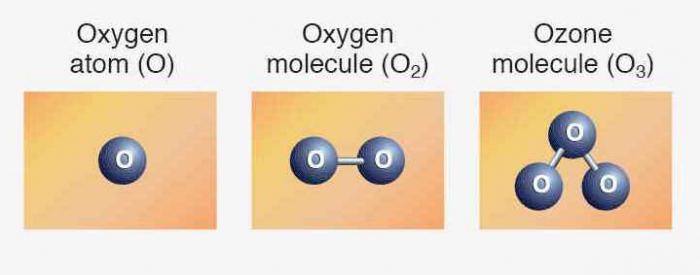
Елементам відповідають прості речовини: кисень, сірка, селен, телур і полоній. Перші три представника виявляють неметалічні властивості. Формула кисню 2. Алотропні видозміни того ж елемента - озон (3). Обидві модифікації є газами. Сірка і селен — тверді неметали. Телур — металлоидное речовина, провідник електричного струму, полоній — метал.
Кисень — найпоширеніший елемент
Загальний вміст атомів елемента в земній корі становить приблизно 47 % (по вазі). Кисень зустрічається як у вільному вигляді, так і в складі численних сполук. Просте речовина, формула якого Про2, знаходиться в складі атмосфери, складаючи 21 % повітря (за обсягом). Молекулярний кисень розчинений у воді, що знаходиться між частинками ґрунту.
Ми вже знаємо, що є інша різновид існування того самого хімічного елемента у формі простої речовини. Це озон — газ, який утворює на висоті близько 30 км від поверхні землі шар, який часто називають озоновим екраном. Зв'язаний кисень входить до молекули води, до складу багатьох гірських порід і мінералів, органічних сполук.
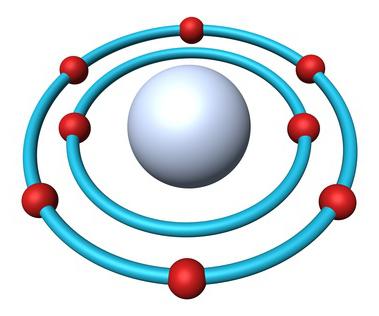
Будова атома кисню
Періодична таблиця Менделєєва містить повну інформацію про кисні:
- Порядковий номер елемента — 8.
- Заряд ядра — +8.
- Загальне число електронів — 8.
- Електронна формула кисню — 1s22s22p4.
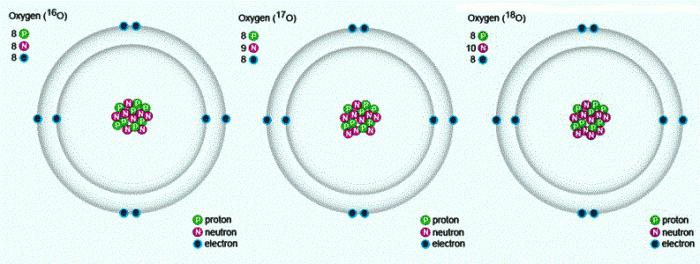
У природі зустрічаються три стабільних ізотопи, які мають однаковий порядковий номер в таблиці Менделєєва, ідентичний склад протонів і електронів, але різне число нейтронів. Позначаються ізотопи одним і тим же символом — О. Для порівняння наведемо схему, що відображає склад трьох ізотопів кисню:
Властивості кисню хімічного елемента
На 2р-підрівні атома є два неспарених електрона, що пояснює появу ступенів окислення –2 і +2. Два спарених електрона не можуть разъединиться, щоб ступінь окислення зросла до +4, у сірки та інших халькогенов. Причина — відсутність вільного підрівня. Тому у сполуках хімічний елемент кисень не проявляє валентність і ступінь окиснення, рівні номеру групи в короткому варіанті періодичної системи (6). Звичайне для нього окислювальне число дорівнює –2.
Тільки в з'єднаннях з фтором кисень проявляє нехарактерну для нього позитивну ступінь окислення +2. Значення ЕО двох сильних неметалів відрізняється: ЕВ (О) = 3,5; ЕО (F) = 4. Як більш електронегативний хімічний елемент, фтор сильніше утримує свої електрони і притягує валентні частинки на зовнішньому енергетичному рівні атома кисню. Тому в реакції з фтором кисень є відновником, віддає електрони.
Кисень — просте речовина
Англійський дослідник Д. Прістлі у 1774 році в ході дослідів виділив газ при розкладанні оксиду ртуті. Двома роками раніше ця ж речовина в чистому вигляді отримав К. Шеєле. Лише через кілька років французький хімік А. Лавуазьє встановив, що за газ входить до складу повітря, вивчив властивості. Хімічна формула кисню 2. Відобразимо в запис складу речовини електрони, що беруть участь в утворенні неполярного ковалентного зв'язку :: О. Замінимокожну зв'язкову електронну пару однією рисою: Про=О. Така формула кисню наочно показує, що атоми в молекулі зв'язані між двома загальними парами електронів.

Виконаємо нескладні розрахунки і визначимо, чому дорівнює відносна молекулярна маса кисню: Mr(O2) = Ar(O) х 2 = 16 х 2 = 32. Для порівняння: Mr(л.) = 29. Хімічна формула кисню відрізняється від формули озону на один атом кисню. Отже, Mr(O3) = Ar(O) х 3 = 48. Озон у 1,5 рази важчий кисню.
Фізичні властивості
Кисень — це газ без кольору, смаку і запаху (при звичайній температурі і тиску, рівному атмосферного). Речовина трохи важчий за повітря; розчиняється у воді, але в невеликих кількостях. Температура плавлення кисню є від'ємною величиною і становить –218,3 °C. Точка, в якій рідкий кисень знову перетворюється в газоподібний, — це його температура кипіння. Для молекул Про2 значення цієї фізичної величини досягає –182,96 °C. В рідкому і твердому стані кисень набуває світло-синє забарвлення.
Одержання кисню в лабораторії
При нагріванні кисневмісних речовин, наприклад перманганату калію, виділяється безбарвний газ, який можна зібрати в колбу або пробірку. Якщо внести в чистий кисень запалену скіпку, то вона горить більш яскраво, ніж у повітрі. Два інших лабораторних способу отримання кисню - розкладання пероксиду водню і хлорату калію (бертолетової солі). Розглянемо схему приладу, який застосовується для термічного розкладання.
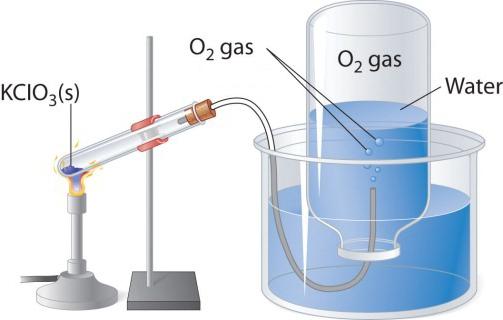
В пробірку або круглодонную колбу треба насипати трохи бертолетової солі, закрити пробкою з газовідвідною трубочкою. Її протилежний кінець слід направити (під водою) перекинуту догори дном колбу. Горлечко повинно бути опущено в широкий стакан або кристалізатор, наповнений водою. Під час нагрівання пробірки з бертолетової сіллю виділяється кисень. За газовідвідній трубці він надходить в колбу, витісняючи з неї воду. Коли колба наповниться газом, її закривають під водою пробкою і перевертають. Отриманий в цьому лабораторному досвіді кисень можна використовувати для вивчення хімічних властивостей простого речовини.
Горіння
Якщо в лабораторії проводиться спалювання речовин в кисні, то потрібно знати і дотримуватися протипожежні правила. Водень миттєво згоряє на повітрі, а змішаний з киснем у співвідношенні 2:1, він вибухонебезпечний. Горіння речовин у чистому кисні відбувається набагато інтенсивніше, ніж у повітрі. Пояснюється це явище складом повітря. Кисень в атмосфері становить трохи більше 1/5 частини (21%). Горіння — це реакція речовин з киснем, у результаті якої утворюються різні продукти, в основному оксиди металів і неметалів. Пожежонебезпечні суміші2 з горючими речовинами, крім того, отримані сполуки можуть бути токсичними.
Горіння звичайної свічки (або сірники) супроводжується утворенням діоксиду вуглецю. Наступний досвід можна провести в домашніх умовах. Якщо спалювати речовина під скляною банкою або великою склянкою, то горіння припиниться, як тільки витратиться весь кисень. Азот не підтримує дихання і горіння. Вуглекислий газ — продукт окислення — більше не вступає в реакцію з киснем. Прозора вапняна вода дозволяє виявити присутність діоксиду вуглецю після горіння свічки. Якщо пропускати продукти горіння через гідроксид кальцію, то розчин каламутніє. Відбувається хімічна реакція між вапняною водою і вуглекислим газом, виходить нерозчинний карбонат кальцію.

Отримання кисню в промислових масштабах
найдешевший процес, у результаті якого виходять вільні від повітря молекули2, не пов'язаний з проведенням хімічних реакцій. У промисловості, наприклад, на металургійних комбінатах, повітря при низькій температурі і високому тиску зріджують. Такі найважливіші компоненти атмосфери, як азот і кисень, киплять при різних температурах. Поділяють повітряну суміш при поступовому нагріванні до звичайної температури. Спочатку виділяються молекули азоту, потім кисню. Спосіб розділення засновано на різних фізичних властивостях простих речовин. Формула простої речовини кисню така ж, як була до охолодження і скраплення повітря, —2.
В результаті деяких реакцій електролізу теж виділяється кисень, його збирають над відповідним електродом. Газ потрібен промисловим, будівельним підприємствам у великих обсягах. Потреби в кисні постійно зростають, особливо потребує в ньому хімічна промисловість. Зберігають отриманий газ для виробничих і медичних цілей в сталевих балонах, забезпечених маркуванням. Ємності з киснем фарбують у синій або блакитний колір, щоб відрізняти від інших зріджених газів — азоту, метану, аміаку.

Хімічні розрахунки за формулою і рівняннями реакцій за участю молекул Про2
Чисельне значення молярної маси кисню збігається з іншого величиною — відносною молекулярною масою. Тільки в першому випадку є одиниці вимірювання. Коротко формула речовини кисню і його молярної маси повинна бути записана так: М (2) = 32 г/моль. При нормальних умовах молюбудь газу відповідає об'єм 22,4 л. Означає, 1 моль Про2 — це 22,4 л речовини 2 моль Про2 44,8 л. За рівнянням реакції між киснем і воднем можна помітити, що взаємодіють 2 моля водню і 1 моль кисню:
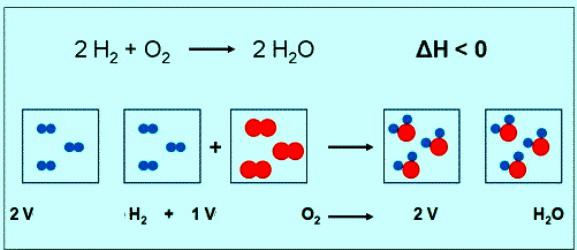
Якщо в реакції бере участь 1 моль водню, то об'єм кисню складе 0,5 моль • 22,4 л/моль = 11,2 л.
Роль молекул Про2 у природі та житті людини
Кисень споживається живими організмами на Землі і бере участь в кругообігу речовин понад 3 млрд років. Це головне речовина для дихання і метаболізму, з його допомогою відбувається розкладання молекул поживних речовин, синтезується необхідна для організмів енергія. Кисень постійно витрачається на Землі, але його запаси поповнюються завдяки фотосинтезу. Російський вчений К. Тімірязєв вважав, що завдяки саме цьому процесу досі існує життя на нашій планеті.

Велика роль кисню в природі і господарстві:
- поглинається в процесі дихання живими організмами;
- бере участь у реакціях фотосинтезу в рослинах;
- входить до складу органічних молекул;
- процеси гниття, бродіння, іржавіння протікають за участю кисню, який виступає в якості окислювача;
- використовується для одержання цінних продуктів органічного синтезу.
Зріджений кисень в балонах використовують для різання і зварювання металів при високих температурах. Ці процеси проводять на машинобудівних заводах, на транспортних і будівельних підприємствах. Для проведення робіт під водою, під землею, на великій висоті в безповітряному просторі люди теж потребують молекулах Про2. Кисневі подушки застосовуються в медицині для збагачення складу повітря, що вдихається хворими людьми. Газ для медичних цілей відрізняється від технічного практично повною відсутністю сторонніх домішок, запаху.

Кисень — ідеальний окислювач
Відомі сполуки кисню з усіма хімічними елементами таблиці Менделєєва, крім перших представників сімейства благородних газів. Багато речовини безпосередньо вступають в реакції з атомами О, виключаючи галогени, золото і платину. Велике значення мають явища з участю кисню, які супроводжуються виділенням світла і тепла. Такі процеси широко використовуються в побуті, промисловості. У металургії взаємодія руд з киснем називають випалюванням. Попередньо подрібнену руду змішують з повітрям, збагаченим киснем. При високих температурах відбувається відновлення металів з сульфідів до простих речовин. Так отримують залізо і деякі кольорові метали. Присутність чистого кисню підвищує швидкість технологічних процесів в різних галузях хімії, техніці та металургії.
Поява дешевого способу отримання кисню з повітря методом поділу на компоненти при низькій температурі стимулювало розвиток багатьох напрямків промислового виробництва. Хіміки вважають молекули2 і атоми Про ідеальними окислювальними агентами. Це природні матеріали, вони постійно відновлюються в природу, не забруднюють навколишнє середовище. Крім того, хімічні реакції з участю кисню найчастіше завершуються синтезом ще одного натурального та безпечного продукту — води. Велика роль2 у знешкодженні токсичних виробничих відходів, очищення води від забруднень. Крім кисню, для знезараження використовується його аллотропная модифікація — озон. Це просте речовина володіє високою окисної активністю. При озонуванні води розкладаються забруднюючі речовини. Озон також згубно діє на хвороботворну мікрофлору.
Article in other languages:
KK: https://tostpost.com/kk/b-l-m/20346-formulasy-otteg-mendeleevt-periodty-kestes---otteg.html
PL: https://tostpost.com/pl/edukacja/20321-formu-a-tlenu-uk-ad-okresowy-mendelejewa---tlen.html
TR: https://tostpost.com/tr/e-itim/20355-form-l-oksijen-periyodik-tablo-periyodik---oksijen.html

Alin Trodden - автор статті, редактор
"Привіт, Я Алін Тродден. Я пишу тексти, читаю книги і шукаю враження. І я непогано вмію розповідати вам про це. Я завжди радий брати участь у цікавих проектах."
Новини
Харун ар-Рашид: цілі, досягнення, супротивники. Правління Харуна ар-Рашида
Друга половина 8 століття нашої ери ознаменувалася ослабленням центральної влади, і віддалені райони Халіфату отримали новий поштовх до розвитку. На тлі загальних змін особливо виділявся Багдад. Досить швидко він перетворився в ку...
Високе Середньовіччя: мистецтво та культура
Високе Середньовіччя - один з визначальних періодів в історії людства. У ті далекі і темні часи формувалася сучасна цивілізація. Зникали стародавні звичаї і з'являлися нові. Значно збільшилася чисельність населення. Відбувся культ...
Хабарництво - це наше минуле чи теперішнє?
Сьогодні ми поговоримо про застарілому слові, яке давно пішло з повсякденного вжитку звичайної людини. Час йде вперед і багато слів стають архаїзмами, які не приживаються в новому середовищі. Найцікавіше полягає в тому, що явище, ...
Сумський державний університет: адреси, факультети, спеціальності
Сумський державний університет – це одне з вищих навчальних закладів України. ВУЗ має досить високі позиції в міжнародних рейтингах. Розташований університет р. Суми (місто є головним в області). Навчання ведеться по багатьо...
Чоловік: систематика та характерні ознаки в будові організму
Особливе місце в системі органічного світу займає людина. Систематика цього виду має свої особливості. Пов'язані вони з біосоціальною основою Людини розумної.Людина: систематикаЗ одного боку, людина є об'єктом живої природи, предс...
Твір "Мій улюблений учитель" для школярів
У школі учням нерідко дають завдання написати твір на різні тематики. Таке творче завдання цікаво і дає можливість повною мірою проявити фантазію і розповісти про те, що на душі. Твір «Мій улюблений учитель» обов'язков...





















Примітка (0)
Ця стаття не має коментарів, будьте першим!